题目内容
17.一定质量的酒精(C2H5OH)不完全燃烧,生成一氧化碳、二氧化碳和水蒸气的混合气体59g,经测定混合气体中氢元素的质量为3g,则参加反应的氧气的质量是( )| A. | 36g | B. | 48g | C. | 64g | D. | 80g |
分析 由题意,一定质量的酒精不完全燃烧,生成一氧化碳、二氧化碳和水蒸气的混合气体59g,经测定混合气体中氢元素的质量为3g,根据质量守恒定律,反应前后元素质量不变,则可确定酒精中氢元素的质量,由酒精中碳元素和氢元素的质量比,可计算出碳元素的质量(即为生成的混合气体中碳元素的质量),则混合气体的质量减去碳元素、氢元素的质量为氧元素的质量据此进行分析判断.
解答 解:一定质量的酒精不完全燃烧,生成一氧化碳、二氧化碳和水蒸气的混合气体59g,经测定混合气体中氢元素的质量为3g;质量守恒定律,反应前后元素质量不变,则酒精中氢元素的质量为3g;酒精中碳元素和氢元素的质量比为(12×2):(1×6)=4:1,则酒精中碳元素的质量为4×3g=12g,即生成的混合气体中碳元素的质量为12g;则酒精中氧元素和氢元素的质量比为16:6=8:3;则酒精中氧元素的质量为:8g; 则混合气体氧元素的质量为59g-12g-3g-8g=36g,即参加反应的氧气的质量为36g.
故选:A.
点评 本题难度不大,掌握质量守恒定律、化学式的有关计算并能灵活运用是正确解答本题的关键.

练习册系列答案
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案
相关题目
16.下列实验方案不能达到预期目的是( )
| A. | 用铜、空气、稀硫酸等原料制取硫酸铜 | |
| B. | 实验室常用石灰石与稀硫酸反应制取大量二氧化碳气体 | |
| C. | 只用一种试剂就能把稀盐酸、BaCl2溶液和KNO3溶液一次性鉴别出来 | |
| D. | 若除去CaCl2溶液中混有的少量稀盐酸,可加入过量CaCO3充分反应后过滤 |
5.下列有关营养素的说法正确的是( )
| A. | 蛋白质是一切生命活动的物质基础 | B. | 纤维素在人体中能够转化为葡萄糖 | ||
| C. | 大多数维生素不需要从食物中摄取 | D. | 过量的碳水化合物不会转化为脂肪 |
12.如图为汽车尾气净化装置中发生反应的微观示意图,下列有关叙述正确的是( )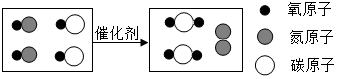

| A. | 该反应属于置换反应 | B. | 图中单质的化学式为O2 | ||
| C. | 反应后分子总数减少 | D. | 反应后氧原子个数减少 |
6.下列有关物质的鉴别方法,其中不正确的是( )
| A. | 用二氧化锰鉴别水和双氧水 | |
| B. | 观察颜色、闻气味鉴别软水和硬水 | |
| C. | 灼烧闻气味鉴别羊毛和尼龙 | |
| D. | 用水鉴别氢氧化钠和氯化钠两种白色固体 |
7.下列实验现象描述正确的是( )
| A. | 点燃纯棉纤维能闻到烧焦羽毛气味 | |
| B. | 铜片投入到稀硫酸中产生大量的气泡 | |
| C. | 硫在空气中燃烧产生淡蓝色火焰,并生成有刺激性气味的气体 | |
| D. | 打开盛有浓盐酸的试剂瓶盖,瓶口有白烟 |