题目内容
4.下列除去混合物中少量杂质的方法或加入试剂合理的是( )| 选项 | 物质 | 所含杂质 | 除去杂质的方法或加入试剂 |
| A | CO气体 | CO2 | 通过灼热的氧化铜 |
| B | CO2气体 | HCl | 通过盛有NaOH溶液的洗气瓶,然后干燥 |
| C | Ca(OH)2 | CaCO3 | 适量盐酸 |
| D | NaCl固体 | Na2SO4 | 溶解后加适量氯化钡溶液,过滤,蒸干 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、CO气体能与灼热的氧化铜反应生成铜和二氧化碳,反而会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
B、CO2和HCl气体均能与NaOH溶液反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
C、Ca(OH)2和CaCO3均能与盐酸反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
D、溶解后,Na2SO4能与适量氯化钡溶液反应生成硫酸钡沉淀和氯化钠,再过滤,蒸干,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
故选:D.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
14.以下关于物质构成的说法中不正确的是( )
| A. | 氯化钠是由钠离子和氯离子构成的 | B. | 汞是由汞原子构成的 | ||
| C. | 干冰是由碳原子和氧原子构成的 | D. | 金刚石是由碳原子构成的 |
14.人类社会的发展离不开能源.当今社会人类利用的能源主要来自化石燃料.回答下列问题:
(1)用来驱动汽车、飞机和轮船的燃料主要是从石油中根据不同沸点范围分馏出来的汽油、航空煤油、柴油等,石油分馏的过程属于物理变化,化石燃料中主要含有碳、氢元素,它完全燃烧的产物是二氧化碳和水,此外还含有硫、氮等元素,它们燃烧时会转化为二氧化硫和氮氧化物,造成空气污染.
(2)我国煤炭资源丰富,煤的综合利用措施主要有煤的气化、焦化和液化,在煤的综合利用中,改变煤的组成和结构的过程属于化学变化.
(3)城市居民生活用燃料主要有液化石油气、天然气和煤气,下表是几种气体燃料的价格和热值:
综合考虑以上因素,你将选用哪种燃料?天然气;理由是天然气的热值高,价格相对较低,对环境污染较小.
(1)用来驱动汽车、飞机和轮船的燃料主要是从石油中根据不同沸点范围分馏出来的汽油、航空煤油、柴油等,石油分馏的过程属于物理变化,化石燃料中主要含有碳、氢元素,它完全燃烧的产物是二氧化碳和水,此外还含有硫、氮等元素,它们燃烧时会转化为二氧化硫和氮氧化物,造成空气污染.
(2)我国煤炭资源丰富,煤的综合利用措施主要有煤的气化、焦化和液化,在煤的综合利用中,改变煤的组成和结构的过程属于化学变化.
(3)城市居民生活用燃料主要有液化石油气、天然气和煤气,下表是几种气体燃料的价格和热值:
| 燃料名称 | 煤气 | 液化石油气 | 天然气 |
| 价格 | 4.2元/千克 | 8.4元/千克 | 4.8元/千克 |
| 热值 | 1.56×104kJ/kg | 4.5×104kJ/kg | 3.9×104kJ/kg |
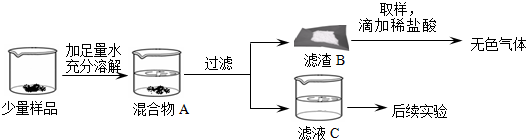
 如图是去除粗盐中难溶性杂质的实验,请回答:
如图是去除粗盐中难溶性杂质的实验,请回答: