题目内容
8.取氯酸钾和二氧化锰的混合物26克,加热至混合物固体质量不再减少为止,冷却后剩余固体质量为16.4g,将剩余固体加入一定量的水中,充分搅拌后过滤,得到溶质质量分数为10%的氯化钾溶液.请计算:(1)氯酸钾的质量;
(2)所得氯化钾溶液的质量.
分析 根据质量守恒定律可知,过程中质量的减少是因为生成了氧气,所以可以求算氧气的质量,根据氧气的质量和对应的化学方程式求算氯化钾和氯酸钾的质量,进而求算对应的质量分数.
解答 解:
根据质量守恒定律可得,生成氧气的质量为26g-16.4g=9.6g
设参加反应的氯酸钾的质量为x,生成的氯化钾的质量为y
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
245 149 96
x y 9.6g
$\frac{245}{x}$=$\frac{149}{y}$=$\frac{96}{9.6g}$
x=24.5g
y=14.9g
所得氯化钾溶液的质量为14.9g÷10%=149g
答:(1)氯酸钾的质量为24.5g
(2)所得氯化钾溶液的质量为149g.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.

练习册系列答案
相关题目
16.下列物质中属于纯净物的是( )
| A. | 加碘食盐 | B. | 烧碱 | C. | 矿泉水 | D. | 浓硫酸 |
3.下列除杂设计(括号内为杂质)所选试剂和操作都正确的是( )
| A. | Fe(Cu) 加入足量稀硫酸,过滤,洗涤、干燥 | |
| B. | Na2CO3(CaCO3) 加入足量水,过滤、蒸发结晶 | |
| C. | KNO3溶液(KOH) 加入适量CuSO4溶液,过滤 | |
| D. | H2(O2) 通过足量灼热的铜网 |
13.下列有关水的净化和处理,说法正确的是( )
| A. | 生活污水应集中处理,达标后再排放 | |
| B. | 过滤能除去水中所有的杂质 | |
| C. | 硬水经活性炭吸附后变成软水 | |
| D. | 电解水生成氢气和氧气的质量比约为2:1 |
17.推理是化学学习中常用的思维方法,下列推理正确的是( )
| A. | CO2和SO2都能和NaOH溶液反应,CO也能和NaOH溶液反应 | |
| B. | CO和C都能和CuO反应生成Cu,有还原性,H2也能和CuO反应生成Cu,也有还原性 | |
| C. | 活泼金属和盐酸反应生成气体,和盐酸反应生成气体的物质是活泼金属 | |
| D. | 氢氧化钙和氢氧化钠都属于碱,都含有金属元素,所以碱都含有金属元素 |
18.实验室有一瓶标签脱落的固体试剂,现分别取少量的该固体进行下列实验,根据实验现象判断,该固体最可能是( )
| 实验操作 | 实验现象 |
| 取该固体于试管中,加水、振荡 | 固体不溶解 |
| 取该固体于试管中,加盐酸、振荡 | 固体溶解,无气泡产生 |
| 一氧化碳通过炽热的该固体,称固体质量、检测尾气 | 固体质量减轻,尾气中只检测到CO与CO2 |
| A. | 碱 | B. | 盐 | C. | 金属单质 | D. | 金属氧化物 |
 向硫酸铁溶液中投入一小块金属钠,反应剧烈,产生如图现象:
向硫酸铁溶液中投入一小块金属钠,反应剧烈,产生如图现象: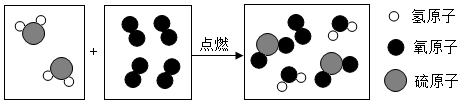
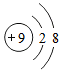 是某微粒的结构示意图,其符号为F-;
是某微粒的结构示意图,其符号为F-;