题目内容
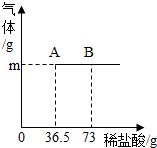 为测定某纯碱(Na2CO3)样品中(含有少量的氯化钠杂质)碳酸钠的质量分数,现称取6g试样放在烧杯中并滴入稀盐酸,当稀盐酸滴加至36.5g时,烧杯内溶液的总质量为40.3g(产生的气体全部逸出).产生气体的质量与滴入稀盐酸的质量关系如图所示,试计算:
为测定某纯碱(Na2CO3)样品中(含有少量的氯化钠杂质)碳酸钠的质量分数,现称取6g试样放在烧杯中并滴入稀盐酸,当稀盐酸滴加至36.5g时,烧杯内溶液的总质量为40.3g(产生的气体全部逸出).产生气体的质量与滴入稀盐酸的质量关系如图所示,试计算:(1)A点产生气体的质量为
2.2g
2.2g
;(2)试样中碳酸钠的质量分数(结果精确到0.1%);
(3)A点时生成物溶液的溶质质量分数(结果精确到0.1%);
(4)B点时,烧杯内溶液中溶质的化学式
NaCl、HCl
NaCl、HCl
.分析:(1)据图可知到A点时盐酸和碳酸钠恰好完全反应,生成气体的质量正好是烧杯中的物质前后减少的质量;
(2)利用碳酸钠与盐酸反应的化学方程式,根据二氧化碳的质量求出碳酸钠的质量,再根据
×100%求出试样中碳酸钠的质量分数;
(3)A点时盐酸和碳酸钠恰好完全反应,生成物溶液是氯化钠溶液,溶液中溶质既包括生成的氯化钠,还包括试液中的氯化钠,并据溶质的质量分数计算式计算此时溶液溶质的质量分数;
(4)到B点时,碳酸钠已反应完,还有剩余的盐酸,因而此时溶液中的溶质除了反应生成的溶质外还有剩余的盐酸中的溶质.
(2)利用碳酸钠与盐酸反应的化学方程式,根据二氧化碳的质量求出碳酸钠的质量,再根据
| 碳酸钠的质量 |
| 试液的质量 |
(3)A点时盐酸和碳酸钠恰好完全反应,生成物溶液是氯化钠溶液,溶液中溶质既包括生成的氯化钠,还包括试液中的氯化钠,并据溶质的质量分数计算式计算此时溶液溶质的质量分数;
(4)到B点时,碳酸钠已反应完,还有剩余的盐酸,因而此时溶液中的溶质除了反应生成的溶质外还有剩余的盐酸中的溶质.
解答:解:(1)A点产生气体的质量为:6g+36.5g-40.3g=2.2g;
(2)设6g试样中Na2CO3质量为x,生成氯化钠的质量是y
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 117 44
x y 2.2g
=
x=5.3g
=
y=5.85g
试样中Na2CO3的质量分数=
×100%≈88.3%
(3)答:试样中Na2CO3的质量分数为88.3%.
(3)试液中氯化钠的质量是6g-5.3g=0.7g,所以A点时生成物溶液的溶质质量分数:
×100%≈16.3%;
(4)当碳酸钠和盐酸恰好完全反应时,溶液中的溶质是氯化钠,但到B点时盐酸已过量,溶液中的溶质除了有氯化钠外还有盐酸中的溶质氯化氢;
故答案为:(1)2.2g;
(2)试样中Na2CO3的质量分数为88.3%;(3)A点时生成物溶液的溶质质量分数16.3%;(4)NaCl、HCl.
(2)设6g试样中Na2CO3质量为x,生成氯化钠的质量是y
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 117 44
x y 2.2g
| 106 |
| x |
| 44 |
| 2.2g |
| 117 |
| y |
| 44 |
| 2.2g |
试样中Na2CO3的质量分数=
| 5.3g |
| 6g |
(3)答:试样中Na2CO3的质量分数为88.3%.
(3)试液中氯化钠的质量是6g-5.3g=0.7g,所以A点时生成物溶液的溶质质量分数:
| 0.7g+5.85g |
| 40.3g |
(4)当碳酸钠和盐酸恰好完全反应时,溶液中的溶质是氯化钠,但到B点时盐酸已过量,溶液中的溶质除了有氯化钠外还有盐酸中的溶质氯化氢;
故答案为:(1)2.2g;
(2)试样中Na2CO3的质量分数为88.3%;(3)A点时生成物溶液的溶质质量分数16.3%;(4)NaCl、HCl.
点评:本题主要考查了根据图象分析已知量并根据化学方程式进行相关方面计算,分析反应后溶液溶质质量分数时,要考虑试液中的杂质是否是溶质的一部分.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 用“侯氏联合制碱法”制得的纯碱常含有少量的氯化钠.为测定某纯碱样品中碳酸钠的含量,小明称取该纯碱样品10g溶解于水中,再滴加氯化钙溶液,产生沉淀的质量如图所示,求:该纯碱样品中碳酸钠的质量分数.
用“侯氏联合制碱法”制得的纯碱常含有少量的氯化钠.为测定某纯碱样品中碳酸钠的含量,小明称取该纯碱样品10g溶解于水中,再滴加氯化钙溶液,产生沉淀的质量如图所示,求:该纯碱样品中碳酸钠的质量分数. 为测定某纯碱(Na2CO3)样品中(含有少量的氯化钠杂质)碳酸钠的质量分数,现称取6g试样放在烧杯中并滴入稀盐酸,当稀盐酸滴加至36.5g时,烧杯内溶液的总质量为40.3g(产生的气体全部逸出).产生气体的质量与滴入稀盐酸的质量关系如图所示.
为测定某纯碱(Na2CO3)样品中(含有少量的氯化钠杂质)碳酸钠的质量分数,现称取6g试样放在烧杯中并滴入稀盐酸,当稀盐酸滴加至36.5g时,烧杯内溶液的总质量为40.3g(产生的气体全部逸出).产生气体的质量与滴入稀盐酸的质量关系如图所示.
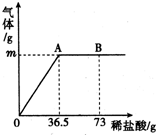 为测定某纯碱样品中(含有少量的氯化钠杂质)碳酸钠的质量分数,现称取6g试样放在烧杯中并滴入稀盐酸,当稀盐酸滴加至36.5g时,烧杯内溶液的总质量为40.3g(产生的气体全部逸出).产生气体的质量与滴入稀盐酸的质量关系如图所示,试计算:
为测定某纯碱样品中(含有少量的氯化钠杂质)碳酸钠的质量分数,现称取6g试样放在烧杯中并滴入稀盐酸,当稀盐酸滴加至36.5g时,烧杯内溶液的总质量为40.3g(产生的气体全部逸出).产生气体的质量与滴入稀盐酸的质量关系如图所示,试计算: