题目内容
17.已知木炭还原氧化铜实验中发生的主要反应:C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑.化学兴趣小组对该实验产物(假设反应物已完全反应)作如下探究:探究一:检验产物的成份
提出问题:实验产物是暗红色固体,很难观察到紫红色固体.暗红色固体是什么?
查阅资料:氧化亚铜(Cu2O)为红色固体;Cu2O+H2SO4═CuSO4+Cu+H2O.
猜想与假设:暗红色固体除铜外还可能含有Cu2O.
设计实验:取少量暗红色固体,加入稀硫酸,如果观察到现象:固体部分溶解,溶液变成蓝色,说明暗红色固体含有Cu2O.
探究二:测定产物中Cu2O的含量
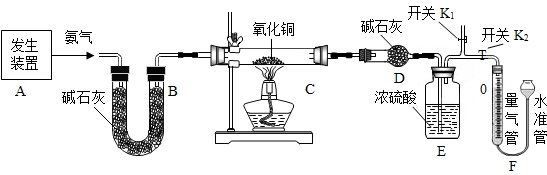
原理:Cu2O+H2$\frac{\underline{\;\;△\;\;}}{\;}$2Cu+H2O,称取一定质量的固体样品,用如图装置进行实验(固定装置略去,碱石灰为氧化钙和氢氧化钠的混合物,可吸收水和酸性物质),通过测定反应前后装置d的质量达到实验目的.
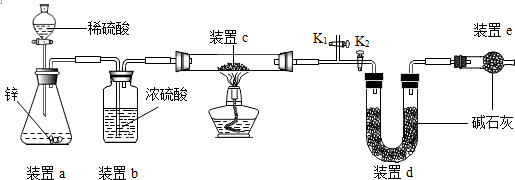
(1)装置a中用稀硫酸而不用稀盐酸,原因是盐酸挥发出氯化氢气体,与d中的物质反应,影响测定结果;
(2)若不加装置e,实验结果会偏高,原因是d中的碱石灰能够吸收空气中的水和二氧化碳;
(3)点燃酒精灯前涉及的部分操作如下,正确的顺序是③②④①
①打开K2,关闭K1 ②检查装置的气密性 ③连接仪器 ④关闭K2,打开K1,通氢气一段时间
(4)还可通过测定反应前后装置c(填“a”、“b”或“c”)的质量达到实验目的.
分析 探究一:
如果暗红色固体中含有Cu2O,加入稀硫酸时,Cu2O和稀硫酸反应生成硫酸铜,硫酸铜溶液是蓝色的;
探究二:
(1)盐酸易挥发,容易挥发出氯化氢气体;
(2)空气中含有水蒸气和二氧化碳,能够被碱石灰吸收;
(3)正确的顺序是:先连接仪器,检查装置的气密性,再关闭K2,打开K1,通氢气一段时间,把装置中的水蒸气和二氧化碳排出,再打开K2,关闭K1,点燃酒精灯;
(4)通过测定反应前后c装置的质量也可以达到实验目的.
解答 解:探究一:
【设计实验】取少量暗红色固体,加入稀硫酸,如果观察到固体部分溶解,溶液变成蓝色,说明暗红色固体含有Cu2O.
故填:固体部分溶解,溶液变成蓝色.
探究二:
(1)装置a中用稀硫酸而不用稀盐酸,原因是盐酸易挥发,挥发出的氯化氢能被碱石灰吸收,影响测定结果.
故填:盐酸挥发出氯化氢气体,与d中的物质反应,影响测定结果.
(2)若不加装置e,实验结果会偏高,原因是d中的碱石灰能够吸收空气中的水和二氧化碳,从而使测定的水的质量偏高,会导致计算的Cu2O的质量偏高,从而导致实验结果会偏高.
故填:d中的碱石灰能够吸收空气中的水和二氧化碳.
(3)点燃酒精灯前涉及的部分操作如下,正确的顺序是:先连接仪器,检查装置的气密性,再关闭K2,打开K1,通氢气一段时间,把装置中的水蒸气和二氧化碳排出,再打开K2,关闭K1,点燃酒精灯.
故填:③②④①.
(4)还可通过测定反应前后装置c的质量达到实验目的,反应前后装置c的质量差即为Cu2O中氧元素的质量,根据氧元素的质量可以计算Cu2O的质量,进一步可以计算产物中Cu2O的含量.
故填:c.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

| A. | 1:97 | B. | 2:97 | C. | 3:97 | D. | 4:97 |
| A. | CO2 (O2)--将混合气体通入灼热的铜网 | |
| B. | MnO2粉末(KCl)--溶解、过滤、洗涤、干燥 | |
| C. | FeSO4溶液(CuSO4)--加入足量锌粉、过滤 | |
| D. | Fe粉(Cu粉)--加入足量稀盐酸、过滤、洗涤、干燥 |
 已知某金属粉末中除含有Fe外还含有一定量的Cu,为测定其中Fe的质量分数,某化学兴趣小组的同学展开了如下的实验探究.
已知某金属粉末中除含有Fe外还含有一定量的Cu,为测定其中Fe的质量分数,某化学兴趣小组的同学展开了如下的实验探究. 取20g该金属粉末,把100g稀硫酸平均分成5份依次加入,充分反应后,过滤出固体,将其洗涤、干燥、称量.实验过程中得到的部分数据与图象如下:
| 加NaOH溶液的次数 | 第一次 | 第二次 | 第三次 | … |
| 剩余固体的质量/g | 16.5 | n | 9.5 | … |
(2)该金属粉末中Fe的质量分数为70%;
(3)第三次加稀硫酸时,完全反应后共生成的氢气质量是多少?(结果保留三位小数)
 请结合如图实验常用装置,回答有关问题.
请结合如图实验常用装置,回答有关问题.