题目内容
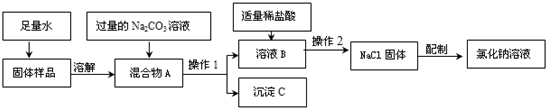
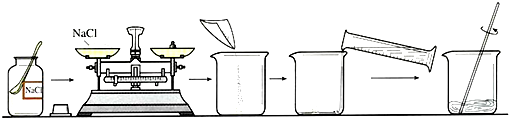
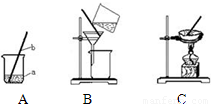
粗盐初步提纯的操作步骤如图所示,相关说法错误的是

- A.溶解时玻璃棒用于搅拌
- B.过滤时玻璃棒用于引流
- C.蒸发至滤液被蒸干后再移去酒精灯
- D.图中“操作1”是称量
C
分析:A、根据溶解操作所需的仪器进行分析判断.
B、根据过滤操作中玻璃棒的作用进行分析判断.
C、根据蒸发操作停止加热的时机进行分析判断.
D、根据粗盐提纯的步骤进行分析判断.
解答:A、溶解时玻璃棒用于搅拌,以加快食盐溶解速率,故选项说法正确.
B、过滤时沿玻璃棒倾倒待过滤的液体,玻璃棒具有引流的作用,故选项说法正确.
C、蒸发时,待蒸发皿中出现较多量的固体时,移去酒精灯停止加热,故选项说法错误.
D、粗盐提纯时应先进行称量,再进行溶解、过滤、蒸发等,“操作1”是称量,故选项说法正确.
故选C.
点评:本题难度不大,掌握粗盐提纯的步骤、各操作的所需仪器与注意事项等是正确解答本题的关键.
分析:A、根据溶解操作所需的仪器进行分析判断.
B、根据过滤操作中玻璃棒的作用进行分析判断.
C、根据蒸发操作停止加热的时机进行分析判断.
D、根据粗盐提纯的步骤进行分析判断.
解答:A、溶解时玻璃棒用于搅拌,以加快食盐溶解速率,故选项说法正确.
B、过滤时沿玻璃棒倾倒待过滤的液体,玻璃棒具有引流的作用,故选项说法正确.
C、蒸发时,待蒸发皿中出现较多量的固体时,移去酒精灯停止加热,故选项说法错误.
D、粗盐提纯时应先进行称量,再进行溶解、过滤、蒸发等,“操作1”是称量,故选项说法正确.
故选C.
点评:本题难度不大,掌握粗盐提纯的步骤、各操作的所需仪器与注意事项等是正确解答本题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
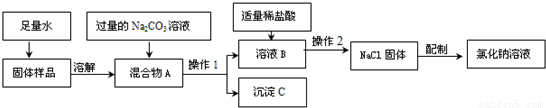
粗盐中含有较多量的可溶性杂质(MgCl2、CaCl2)和不溶性杂质(泥沙等).某兴趣小组设计出下列粗盐提纯的实验方案,请你一起来完成.
(1)下图为粗盐初步提纯的部分操作示意图,请用图示编号依据操作步骤的先后顺序进行填空.


①溶解________;②过滤________;③蒸发________;④计算产率________.
(2)分析以上实验可能出现误差的原因(答一点)________.
(3)小组中的甲乙二位同学为除去粗盐中可溶性杂质,甲用饱和食盐水洗涤,乙选择适当试剂通过反应除去杂质.乙先将粗盐全部溶解,然后加试剂进行除杂反应,待反应完全后,再将食盐水蒸干得到精盐.请你参与乙同学反应除杂的部分方案设计.
可供选用的物质有:Ca(OH)2溶液、NaOH溶液、饱和Na2CO3溶液、饱和NaCl溶液.
| 实 验 步 骤 | 现 象 | 结 论 和 化 学 方 程 式 |
| ①取少量水样于试管中,向其中滴加Ca(OH)2溶液,直到不再产生沉淀 | 有白色沉淀产生 | MgCl2+Ca(OH)2=Mg(OH)2↓+CaCl2 |
| ②继续向上述试管中滴加,直到不再产生沉淀 | 有白色沉淀产生 | 化学方程式: |
| ③过滤 | 滤液澄清 |
(2009?溧水县一模)粗盐中含有较多量的可溶性杂质(MgCl2、CaCl2)和不溶性杂质(泥沙等).某兴趣小组设计出下列粗盐提纯的实验方案,请你一起来完成.
(1)下图为粗盐初步提纯的部分操作示意图,请用图示编号依据操作步骤的先后顺序进行填空.


①溶解______;②过滤______;③蒸发______;④计算产率______.
(2)分析以上实验可能出现误差的原因(答一点)______.
(3)小组中的甲乙二位同学为除去粗盐中可溶性杂质,甲用饱和食盐水洗涤,乙选择适当试剂通过反应除去杂质.乙先将粗盐全部溶解,然后加试剂进行除杂反应,待反应完全后,再将食盐水蒸干得到精盐.请你参与乙同学反应除杂的部分方案设计.
可供选用的物质有:Ca(OH)2溶液、NaOH溶液、饱和Na2CO3溶液、饱和NaCl溶液.
(1)下图为粗盐初步提纯的部分操作示意图,请用图示编号依据操作步骤的先后顺序进行填空.


①溶解______;②过滤______;③蒸发______;④计算产率______.
(2)分析以上实验可能出现误差的原因(答一点)______.
(3)小组中的甲乙二位同学为除去粗盐中可溶性杂质,甲用饱和食盐水洗涤,乙选择适当试剂通过反应除去杂质.乙先将粗盐全部溶解,然后加试剂进行除杂反应,待反应完全后,再将食盐水蒸干得到精盐.请你参与乙同学反应除杂的部分方案设计.
可供选用的物质有:Ca(OH)2溶液、NaOH溶液、饱和Na2CO3溶液、饱和NaCl溶液.
| 实 验 步 骤 | 现 象 | 结 论 和 化 学 方 程 式 |
| ①取少量水样于试管中,向其中滴加Ca(OH)2溶液,直到不再产生沉淀 | 有白色沉淀产生 | MgCl2+Ca(OH)2=Mg(OH)2↓+CaCl2 |
| ②继续向上述试管中滴加______,直到不再产生沉淀 | 有白色沉淀产生 | 化学方程式: ______ |
| ③过滤 | 滤液澄清 |

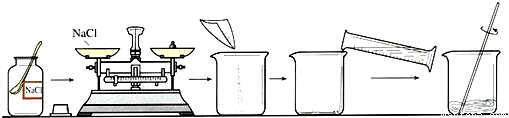
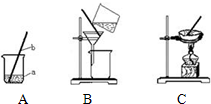 (1)在做粗盐初步提纯的实验时,要进行如图所示的实验操作.
(1)在做粗盐初步提纯的实验时,要进行如图所示的实验操作.