题目内容
1. 某化学兴趣小组的同学通过实验研究了两个问题.
某化学兴趣小组的同学通过实验研究了两个问题.步骤1:探究燃烧条件
步骤1:在C中加入少量白磷并加入热水,塞好胶塞使导管口进入热水中发现白磷不燃烧;
步骤2:打开K1,关闭K2,将A中的溶液滴入B中,C中有气泡冒出,白磷燃烧,B中发生的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
通过以上实验研究了燃烧的一个条件.它是可燃物充分与氧气接触.
实验2:研究CO2与NaOH固体的反应
步骤1:A中盛有稀盐酸、B中Na2CO3固体,C中NaOH固体
打开K1,关闭K2,将A中的溶液滴入B中,气球变大,打开K2,关闭K1,一段时间后气体没有明显弯瘪.
步骤2:依据以上实验现象,改进后重新添加药品,进行实验2.
步骤3:打开K2,关闭K1,将A中液体滴入B中,用燃着的木条放在K2上,发现木条熄灭,问上述操作的目的检验B中是否产生二氧化碳.
然后进行后续实验,说明CO2与NaOH固体发生了反应.
(1)写出CO2与NaOH发生反应的化学方程式CO2+2NaOH=Na2CO3+H2O.
(2)后续实验的操作与现象为打开K2,关闭K1,一段时间后气体明显变瘪.
分析 燃烧的三个条件缺一不可:①物质具有可燃性②可燃物充分与氧气接触③可燃物达到着火点.打开K1,关闭K2,将A中的溶液滴入B中,C中有气泡冒出,白磷燃烧,说明B中产生氧气,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,要注意配平;通过以上实验研究了燃烧的一个条件,它是可燃物充分与氧气接触;打开K2,关闭K1,将A中液体滴入B中,用燃着的木条放在K2上,发现木条熄灭,问上述操作的目的:检验B中是否产生二氧化碳;二氧化碳和氢氧化钠反应生成碳酸钠和水,配平即可;后续实验的操作与现象为:打开K2,关闭K1,一段时间后气体明显变瘪;
解答 解:步骤2:打开K1,关闭K2,将A中的溶液滴入B中,C中有气泡冒出,白磷燃烧,说明B中产生氧气,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,要注意配平;通过以上实验研究了燃烧的一个条件,它是可燃物充分与氧气接触;故答案为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;可燃物充分与氧气接触;
步骤3:打开K2,关闭K1,将A中液体滴入B中,用燃着的木条放在K2上,发现木条熄灭,问上述操作的目的:检验B中是否产生二氧化碳;故答案为:检验B中是否产生二氧化碳;
(1)二氧化碳和氢氧化钠反应生成碳酸钠和水,配平即可;故答案为:CO2+2NaOH=Na2CO3+H2O;
(2)后续实验的操作与现象为:打开K2,关闭K1,一段时间后气体明显变瘪;故答案为:打开K2,关闭K1,一段时间后气体明显变瘪;
点评 实验探究题是近几年中考的重点内容之一,它包括实验方法和过程的探究,实验结论和实验规律的探究等.本题通过查阅资料和实验分析,得到了正确的结论,属于结论性探究.同学们要具体分析,综合掌握,本考点主要出现在实验题中.


(1)装置图中仪器a的名称为集气瓶;
(2)实验室用KMnO4制取O2应选用的一套实验装置为AD或AF(填装置编号)该反应的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)实验室用石灰石和稀盐酸制取二氧化碳的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑;
(4)常温下,可用固体硫化亚铁(FeS)和稀硫酸反应制取硫化氢(H2S)气体,可选择的发生装置是B或C(填装置编号).若用充满水的G装置收集H2,气体从c(填“b”或“c”)处导管进入.
(5)某同学向过氧化氢溶液中加入二氧化锰制取氧气,相关数据如下:
| 反应前物质的质量/g | 充分反应后物质的质量/g | |
| 过氧化氢溶液 | 二氧化锰 | 固体与液体混合物质量 |
| 68.0 | 0.1 | 66.5 |
①该同学制得氧气的质量为多少?
②该同学所用过氧化氢溶液的溶质质量分数为多少?
| A. | NaCl | B. | NaOH | C. | CaCO3 | D. | Na2CO3 |
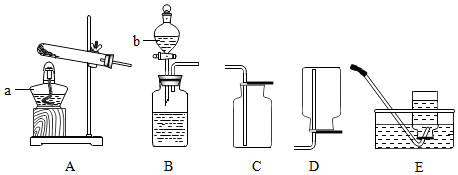
①写出仪器名称:a酒精灯; b分液漏斗;
②用氯酸钾和二氧化锰的混合物制取氧气选择的一套装置是AC或者AE(填字母);其中二氧化锰的作用是催化剂,检验收集的氧气是干燥的方法:加入硫酸铜固体,现象为白色粉末不变蓝,则是干燥的;
③实验中,有很多操作步骤必须严格按要求进行,否则或实验失败或发生危险.
| 必须遵循操作先后的实验 | 先进行的操作 | 后进行的操作 |
| a制取氧气 | 检查装置气密性 | 再向容器中装药品 |
| b氯酸钾制取氧气用排水发收集氧气结束时 | 先将导管从水槽移开 | 熄灭酒精灯 |
| 给药品加热 | 先均匀受热 | 再集中加热 |
⑤同学用制备的一瓶氧气来做铁丝在氧气中的燃烧,将一根铁丝以螺旋状绑在火柴上,点燃火柴后将铁丝慢慢伸入一瓶氧气中,将会看到剧烈燃烧,火星四射,生成黑色固体,放出大量热.但是实际上铁丝只红热一下,没其他现象,请分析铁丝没有燃烧的可能原因没有等到气泡均匀连续就收集或者铁丝表面有锈等(一条即可);
⑥实验室对氯酸钾和二氧化锰混合制氧气后剩余的固体进行了处理:(每步均充分)
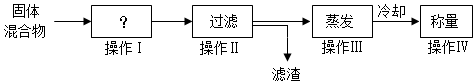
甲、操作Ⅰ的名称及最后称量的固体分析正确的是C
A.称量、二氧化锰 B.溶解、二氧化锰 C.溶解、氯化钾
乙、操作Ⅰ、Ⅱ、III中都用到的玻璃仪器名称是玻璃棒操作Ⅱ中它的作用是引流.
 实验室常用过氧化氢溶液与二氧化锰混合制取氧气,写出有关反应的化学方程式.
实验室常用过氧化氢溶液与二氧化锰混合制取氧气,写出有关反应的化学方程式.【查阅资料】过氧化氢制氧气的催化剂有很多种,如金属氧化物,过氧化氢酶和某些盐类物质等等.
【提出问题】硫酸铜溶液能作过氧化氢制氧气的催化剂吗?如果可以,影响其催化效果的因素有哪些?
【猜想与验证】硫酸铜溶液能作过氧化氢制氧气的催化剂,且其酸碱性对催化效果有影响.
【完成实验】本实验在常温下进行
| 实验编号 | 反应物 | 催化剂 |
| ① | 10mL5%H2O2溶液 | 无 |
| ② | 10mL5%H2O2溶液 | 10滴0.1%CuSO4溶液 |
| ③ | 10mL5%H2O2溶液+少量HCl溶液 | 10滴0.1%CuSO4溶液 |
| ④ | 10mL5%H2O2溶液+少量NaOH溶液 | 10滴0.1%CuSO4溶液 |
(1)由实验①和实验②对比,可以探究CuSO4能够加速过氧化氢溶液的分解.
(2)若要证明CuSO4是该反应的催化剂,还要验证它在化学反应前后质量和化学性质不变.
(3)实验编号②③④中,测得生成氧气的体积随时间变化的关系如图所示.分析该图能够得出的实验结论是硫酸铜溶液能作过氧化氢制氧气的催化剂,且其酸碱性对催化效果有影响.
(4)请你再写出一种影响硫酸铜催化效果的因素硫酸铜溶液的浓度.
【继续探究】请你写出一种影响硫酸铜溶液催化效果的因素(与之前因素不相同),并设计实验进行探究
猜想与验证:温度对硫酸铜溶液催化效果有影响.
实验探究:在不同温度下,取两支试管分别加入相同体积10mL5%的H2O2溶液,加入相同体积和浓度的硫酸铜溶液,比较收集一瓶气体所需要的时间.
 如图是元素周期表中的一格,下面从该图获取的信息中,正确的是( )
如图是元素周期表中的一格,下面从该图获取的信息中,正确的是( )| A. | 该元素的原子序数为52 | B. | 该元素属于非金属元素 | ||
| C. | 该元素相对原子量为52g | D. | 该元素的原子核外有24个电子 |
| A. | 水银-Ag | B. | 金刚石-Au | C. | 干冰-H2O | D. | 食盐-NaCl |
 化学与生活息息相关.
化学与生活息息相关.