题目内容
某有机物在氧气中充分燃烧后,产物只有二氧化碳和水.甲、乙两组同学分别用A、B两种方法测定它的组成,得到两组数据(如下图所示).请你分析,选用的正确方法是________,推测出该有机物是由________元素组成的,各元素的质量比为________(实验过程中气体均全部被吸收).


答案:
解析:
提示:
解析:
|
答案:B,碳、氢、氧,3∶1∶4 【过程探究】A、B两种方法的区别在于二氧化碳和水的吸收顺序不同,首先要判断哪种方法正确,然后再分析实验数据.根据实验数据计算时,要弄清每个数据的化学意义,要步骤清楚、结果正确. A方法不正确,因为混合气体通过氢氧化钠溶液后,其中的二氧化碳被吸收,导出的气体中混入了从氢氧化钠溶液中挥发出的水蒸气;同时,原混合气中的水蒸气遇冷的氢氧化钠溶液会凝聚成水,有部分留在溶液中;这两种原因导致氢氧化钠溶液和浓硫酸的质量增加与被测二氧化碳和水的质量有误差. 根据B方法(乙组)的实验数据可知:燃烧生成水3.6g,二氧化碳4.4g. 该有机物中氢元素的质量= 该有机物中碳元素的质量= 该有机物中氧元素的质量=3.2g-0.4g-1.2g=1.6g(根据质量守恒定律) 计算得该物质中碳、氢、氧元素的质量比为3∶1∶4. |
提示:
|
【设计意图】本题主要检测:①气体检验的顺序,②气体检验与气体除杂、干燥的区别和联系,③实验与计算的简单综合. |

练习册系列答案
相关题目
某有机物在氧气中充分燃烧后,产生只有二氧化碳和水,甲、乙两组同学分别用下图两种方法测定它的组成.请你分析,并参与测定工作;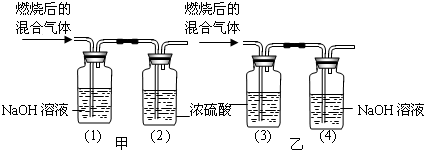
(1)你选用的实验装置是 (“甲”或“乙”),你不选另一个装置的原因是 .
(2)根据表中数据,推测出该有机物是由 元素组成的,各元素的质量比为 (假设实验过程中气体均全部被吸收).
提示:浓硫酸可以吸收水蒸气,氢氧化钠可以吸收二氧化碳.

| 燃烧有机物的质量 | 实验装置 | 实验(1)~(4)装置质量 | ||
| 实验前 | 实验后 | |||
| 甲组 | 1.6g | 甲 | (1)150g | (1)154.6g |
| (2)150g | (1)153.4g | |||
| 乙组 | 1.6g | 乙 | (3)150g | (1)153.6g |
| (4)150g | (1)154.4g | |||
(2)根据表中数据,推测出该有机物是由
提示:浓硫酸可以吸收水蒸气,氢氧化钠可以吸收二氧化碳.
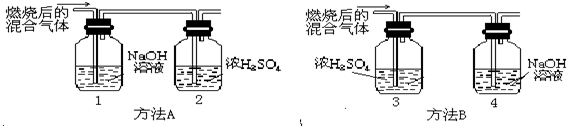
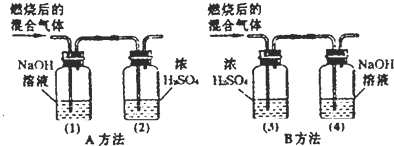 (2005?青浦区)某有机物在氧气中充分燃烧后,产物只有二氧化碳和水.甲、乙两组同学分别用A、两种方法(为如图所示)测定它的组成,得到两组数据(见下表).请你分析:浓H2SO4具有
(2005?青浦区)某有机物在氧气中充分燃烧后,产物只有二氧化碳和水.甲、乙两组同学分别用A、两种方法(为如图所示)测定它的组成,得到两组数据(见下表).请你分析:浓H2SO4具有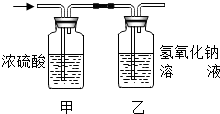 (2012?牡丹江)某有机物在氧气中充分燃烧,将生成的水蒸气、二氧化碳气体依次通过装置甲和乙 (假设每步吸收完全),称量通入气体前后装置的质量,数据如下:
(2012?牡丹江)某有机物在氧气中充分燃烧,将生成的水蒸气、二氧化碳气体依次通过装置甲和乙 (假设每步吸收完全),称量通入气体前后装置的质量,数据如下: