题目内容
14.将纯净的氧化铜粉末装入试管中,称得总质量为48.8g,在加热条件下通入一氧化碳,反应一段时间后,将试管冷却、称量,称得总质量为44g,求反应生成铜的质量.分析 一氧化碳与氧化铜反应生成铜和二氧化碳,由题意,48.8g是氧化铜的质量,由题意,不一定完全反应,即反应后可能有剩余;反应一段时间后所得的固体质量44g,可能铜和剩余的氧化铜的混合物,故不能用44.8g、44g进行解题;反应后固体物质的质量减少了48.8g-44g=4.8g,据此结合固体差量法,进行分析解答.
解答 解:设反应生成铜的质量为x
CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2 固体差量
80 64 80-64=16
x 48.8g-44g=4.8g
$\frac{64}{16}=\frac{x}{4.8g}$ x=19.2g
答:反应生成铜的质量为19.2g.
点评 本题难度不大,考查利用化学方程式的计算,利用固体差量法是正确解答本题的关键和捷径.

练习册系列答案
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
4.2015年11月30日至12月11日,第21届联合国气候变化大会在巴黎举行,其目标是把全球气温在本世纪末的升幅控制在比工业革命前不超过2摄氏度,为达到这一目标,下列措施不可行的是( )
| A. | 发达国家为发展中国家提供资金和技术支持 | |
| B. | 禁止使用煤和石油 | |
| C. | 大力开发太阳能、风能等清洁能源 | |
| D. | 植树造林,严禁乱砍滥伐 |
5.X、Y、Z是金属活动性顺序表里的三种金属,它们在溶液中能发生如下反应:
①X+YSO4═XSO4+Y ②Z+2YNO3═Z(NO3)2+2Y
③X+H2SO4═XSO4+H2↑ ④Z 与H2SO4 不发生反应
则X、Y、Z三种金属的活动性强弱顺序正确的是( )
①X+YSO4═XSO4+Y ②Z+2YNO3═Z(NO3)2+2Y
③X+H2SO4═XSO4+H2↑ ④Z 与H2SO4 不发生反应
则X、Y、Z三种金属的活动性强弱顺序正确的是( )
| A. | X>Y>Z | B. | X>Z>Y | C. | Y>Z>X | D. | Y>X>Z |
19.下列四组的溶液,不另加其它试剂就可将它们区别开来的是( )
| A. | NaOH、HCl、H2SO4 | B. | HCl、NaCl、CuSO4 | ||
| C. | CaCl2、Na2CO3、K2CO3 | D. | NaOH、NaCl、FeCl3 |
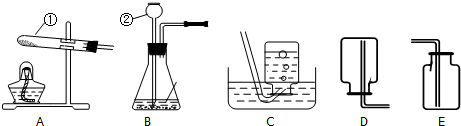
9.下列实验操作或装置正确的是( )
| A. |  收集二氧化碳 | B. | 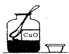 取固体药品 | C. | 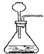 实验室制氧气 | D. | 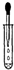 滴加液体 |