题目内容
课外活动小组的同学在测定由NaCl和Na2CO3形成的固体混合物组成时,进行了以下实验:取40 g固体混合物配成溶液,平均分为四份,然后分别加入一定质量分数的CaCl2溶液,实验数据见下表:| | 实验一 | 实验二 | 实验三 | 实验四 |
| 原固体混合物质量 | 10g | 10g | 10g | 10g |
| 加入CaCl2溶液质量 | 10g | 20g | 30g | 40g |
| 生成的沉淀的质量 | 2g | m | 5g | 5g |
(1)生成的沉淀是(填写化学式) 。 (2)10g原固体混合物配成的溶液和足量CaCl2溶液反应,最多生成沉淀质量为 g。
(3)m= g。
(4)原固体混合物中NaCl的质量分数是多少?
(1)CaCO3 (1分) (2)5 (1分) (3) 4 (1分)
(4)CaCl2 + Na2CO3 = CaCO3↓ + 2NaCl
106 100
x 5g ………………………………………………… (1分)
 ………………………………………………… (1分)
………………………………………………… (1分)
x = 5.3g …………………………… (1分)
固体混合物中NaCl的质量分数是: × 100% = 47%
× 100% = 47%
………………… (2分 ,列式和结果各1分)解析:
(1)只有碳酸根离子与钙离子会产生白色沉淀碳酸钙,(2)由表可知10g原固体混合物配成的溶液和足量CaCl2溶液反应,最多生成沉淀质量为5g,(3)分析实验数据可知,每加入10g氯化钙溶液可生成2g沉淀,因此加入20g氯化钙溶液时,得到沉淀质量m=2g× =4g,(4)加入氯化钙溶液至完全反应时,生成沉淀质量为5g,根据碳酸钠与氯化钙反应的化学方程式,可由生成沉淀碳酸钙的质量计算中原固体混合物中Na2CO3的质量,即可求得原固体混合物中NaCl的质量,可求得原固体混合物中NaCl的质量分数.
=4g,(4)加入氯化钙溶液至完全反应时,生成沉淀质量为5g,根据碳酸钠与氯化钙反应的化学方程式,可由生成沉淀碳酸钙的质量计算中原固体混合物中Na2CO3的质量,即可求得原固体混合物中NaCl的质量,可求得原固体混合物中NaCl的质量分数.
(4)CaCl2 + Na2CO3 = CaCO3↓ + 2NaCl
106 100
x 5g ………………………………………………… (1分)
 ………………………………………………… (1分)
………………………………………………… (1分)x = 5.3g …………………………… (1分)
固体混合物中NaCl的质量分数是:
 × 100% = 47%
× 100% = 47%………………… (2分 ,列式和结果各1分)解析:
(1)只有碳酸根离子与钙离子会产生白色沉淀碳酸钙,(2)由表可知10g原固体混合物配成的溶液和足量CaCl2溶液反应,最多生成沉淀质量为5g,(3)分析实验数据可知,每加入10g氯化钙溶液可生成2g沉淀,因此加入20g氯化钙溶液时,得到沉淀质量m=2g×
 =4g,(4)加入氯化钙溶液至完全反应时,生成沉淀质量为5g,根据碳酸钠与氯化钙反应的化学方程式,可由生成沉淀碳酸钙的质量计算中原固体混合物中Na2CO3的质量,即可求得原固体混合物中NaCl的质量,可求得原固体混合物中NaCl的质量分数.
=4g,(4)加入氯化钙溶液至完全反应时,生成沉淀质量为5g,根据碳酸钠与氯化钙反应的化学方程式,可由生成沉淀碳酸钙的质量计算中原固体混合物中Na2CO3的质量,即可求得原固体混合物中NaCl的质量,可求得原固体混合物中NaCl的质量分数. 
练习册系列答案
相关题目
课外活动小组的同学在测定由NaCl和Na2CO3形成的固体混合物组成时,进行了以下实验:取40g固体混合物配成溶液,平均分为四份,然后分别加入一定质量分数的CaCl2溶液,实验数据见下表:
请分析表中数据回答并计算.
(1)m= g.
(2)原固体混合物中Na2CO3的质量分数是多少? .
| 实验一 | 实验二 | 实验三 | 实验四 | |
| 原固体混合物质量 | 10g | 10g | 10g | 10g |
| 加入CaCl2溶液质量 | 10g | 20g | 30g | 40g |
| 生成的沉淀的质量 | 2g | m | 5g | 5g |
(1)m=
(2)原固体混合物中Na2CO3的质量分数是多少?
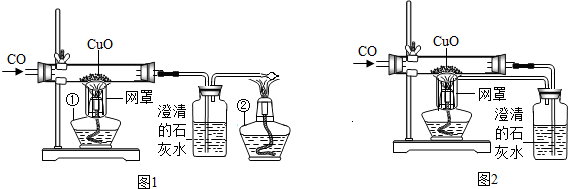
 某校课外活动小组的同学在老师的帮助下,探究用赤铁矿(主要成分Fe2O3)炼铁的主要反应原理.他们设计的实验装置,如图:
某校课外活动小组的同学在老师的帮助下,探究用赤铁矿(主要成分Fe2O3)炼铁的主要反应原理.他们设计的实验装置,如图: