题目内容
 随着人们生活水平的不断提高,汽车已走进千家万户.制造汽车要用到含铜、铁、铝等成分的多种金属材料.
随着人们生活水平的不断提高,汽车已走进千家万户.制造汽车要用到含铜、铁、铝等成分的多种金属材料.(1)在汽车电路中,经常用铜作导线,这是利用了铜的
(2)车体多用钢材制造.其表面喷漆不仅美观,而且可有效防止与
(3)工业上用CO还原赤铁矿(主要成分:氧化铁)冶炼金属铁的化学方程式为
(4)化学兴趣小组的同学欲测定某赤铁矿石中氧化铁的质量分数.
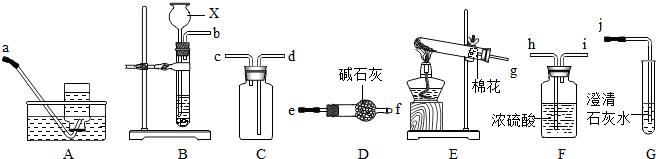
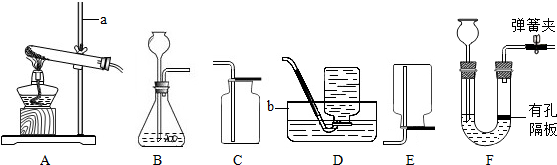
Ⅰ.甲同学取一定质量的赤铁矿粉与过量的木炭粉混合,用如图所示装置(尾气处理部分省略未画)以合理的操作步骤测定(假设杂质始终不发生变化).
①实验中持续通入干燥的氮气.加热前缓缓通入一段时间,其作用是
②反应结束后,甲同学熄灭了喷灯的火焰后,马上停止通入N2,他的操作对吗?请判断并说明理由
③如果氢氧化钠溶液对二氧化碳的吸收是完全的,那么甲同学用氢氧化钠溶液的质量变化测定出氧化铁的质量分数将
Ⅱ.乙同学取矿石样品10g,加入足量稀盐酸,完全反应后,共用去稀盐酸109.5g,过滤得到滤渣2g(假设杂质既不溶于水也不与酸发生反应).请你和乙同学-起计算赤铁矿石中氧化铁的质量分数和反应后溶液中溶质的质量分数.(请写出计算过程)
考点:金属的物理性质及用途,气体的净化(除杂),有关溶质质量分数的简单计算,铁的冶炼,金属锈蚀的条件及其防护,碳的化学性质,根据化学反应方程式的计算
专题:溶质质量分数与化学方程式相结合的计算,金属与金属材料
分析:(1)根据铜用作导线,是因为铜具有良好的导电性进行解答;
(2)根据铁在与氧气和水蒸气同时接触时会生锈,在车体表面喷漆可以防止铁与氧气、水蒸气接触而生锈进行解答;
(3)根据一氧化碳与氧化铁反应生成铁和二氧化碳进行解答;
(4)本题第一问解题的关键在于知道实验探究的目的,用氮气的目的是将装置内的空气排尽;马上停止通入N2不对;b中的NaOH溶液会倒吸入a中造成硬质玻璃管破裂.弄清化学反应中反应物、生成物之间的关系,同时要弄清杂质在反应中存在于什么地方.第二问中关于反应后溶液中溶质的质量分数的计算,关键是要弄清反应后溶液是什么溶液.一般来说,可根据化学方程式求溶质的质量,溶液的质量可根据公式:“反应后溶液的质量=反应前加入的所有物质质量之和-杂质的质量-气体的质量-沉淀的质量”来求出.写化学方程式时一定先分析题意,得出反应物和生成物.根据化学方程式计算时,要分析题目中所给的已知条件是什么,需要求解的是什么,然后再根据相关知识进行解答.
(2)根据铁在与氧气和水蒸气同时接触时会生锈,在车体表面喷漆可以防止铁与氧气、水蒸气接触而生锈进行解答;
(3)根据一氧化碳与氧化铁反应生成铁和二氧化碳进行解答;
(4)本题第一问解题的关键在于知道实验探究的目的,用氮气的目的是将装置内的空气排尽;马上停止通入N2不对;b中的NaOH溶液会倒吸入a中造成硬质玻璃管破裂.弄清化学反应中反应物、生成物之间的关系,同时要弄清杂质在反应中存在于什么地方.第二问中关于反应后溶液中溶质的质量分数的计算,关键是要弄清反应后溶液是什么溶液.一般来说,可根据化学方程式求溶质的质量,溶液的质量可根据公式:“反应后溶液的质量=反应前加入的所有物质质量之和-杂质的质量-气体的质量-沉淀的质量”来求出.写化学方程式时一定先分析题意,得出反应物和生成物.根据化学方程式计算时,要分析题目中所给的已知条件是什么,需要求解的是什么,然后再根据相关知识进行解答.
解答:解:(1)铜用作导线,是因为铜具有良好的导电性;
(2)铁在与氧气和水蒸气同时接触时会生锈,在车体表面喷漆可以防止铁与氧气、水蒸气接触而生锈;
(3)一氧化碳与氧化铁反应生成铁和二氧化碳,反应的化学方程式为3CO+Fe2O3
2Fe+3CO2;
(4)Ⅰ①通氮气主要是隔绝氧气,加热前就通入一段时间是要提前排尽装置内的空气.②熄灭了喷灯的火焰后,马上停止通入氮气,玻璃管内气体压强减小,会出现倒吸现象.③NaOH溶液能吸收CO2,从而能测出CO2的质量,代入化学方程式即可求得氧化铁质量及其质量分数.但装置b还能吸收空气中的二氧化碳气体,使二氧化碳的质量增加,所求氧化铁的质量增大.
Ⅱ.铁矿石的质量分数
×100%=80%
设和8g Fe2O3反应生成FeCl3质量为x.
Fe2O3+6HCl═2FeCl3+3H2O
160 325
8g x
=
X=16.25g
溶液中FeCl3的质量分数
×100%=13.8%
答:赤铁矿石中氧化铁的质量分数和反应后溶液中氯化铁的质量分数分别是80%、13.8%
故答案为:(1)导电;(2)氧气和水;(3)3CO+Fe2O3
2Fe+3CO2
(4)将装置内的空气排尽;不对;b中的NaOH溶液会倒吸入a中造成硬质玻璃管破裂;偏大,
铁矿石的质量分数
×100%=80%
设和8g Fe2O3反应生成FeCl3质量为x.
Fe2O3+6HCl═2FeCl3+3H2O
160 325
8g x
=
X=16.25g
溶液中FeCl3的质量分数
×100%=13.8%
答:赤铁矿石中氧化铁的质量分数和反应后溶液中氯化铁的质量分数分别是80%、13.8%
故答案为:80%; 13.8%
(2)铁在与氧气和水蒸气同时接触时会生锈,在车体表面喷漆可以防止铁与氧气、水蒸气接触而生锈;
(3)一氧化碳与氧化铁反应生成铁和二氧化碳,反应的化学方程式为3CO+Fe2O3
| ||
(4)Ⅰ①通氮气主要是隔绝氧气,加热前就通入一段时间是要提前排尽装置内的空气.②熄灭了喷灯的火焰后,马上停止通入氮气,玻璃管内气体压强减小,会出现倒吸现象.③NaOH溶液能吸收CO2,从而能测出CO2的质量,代入化学方程式即可求得氧化铁质量及其质量分数.但装置b还能吸收空气中的二氧化碳气体,使二氧化碳的质量增加,所求氧化铁的质量增大.
Ⅱ.铁矿石的质量分数
| 10g-2g |
| 10g |
设和8g Fe2O3反应生成FeCl3质量为x.
Fe2O3+6HCl═2FeCl3+3H2O
160 325
8g x
| 160 |
| 8g |
| 325 |
| x |
X=16.25g
溶液中FeCl3的质量分数
| 16.25g |
| 8g+109.5g |
答:赤铁矿石中氧化铁的质量分数和反应后溶液中氯化铁的质量分数分别是80%、13.8%
故答案为:(1)导电;(2)氧气和水;(3)3CO+Fe2O3
| ||
(4)将装置内的空气排尽;不对;b中的NaOH溶液会倒吸入a中造成硬质玻璃管破裂;偏大,
铁矿石的质量分数
| 10g-2g |
| 10g |
设和8g Fe2O3反应生成FeCl3质量为x.
Fe2O3+6HCl═2FeCl3+3H2O
160 325
8g x
| 160 |
| 8g |
| 325 |
| x |
X=16.25g
溶液中FeCl3的质量分数
| 16.25g |
| 8g+109.5g |
答:赤铁矿石中氧化铁的质量分数和反应后溶液中氯化铁的质量分数分别是80%、13.8%
故答案为:80%; 13.8%
点评:本题考查了金属的物理性质以及常见金属的活动性,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
下列物质的分类,对应正确的是( )
| A、混合物:水银、天然气 |
| B、新能源:太阳能、潮汐能 |
| C、合成材料:合金、塑料 |
| D、碳单质:金刚石、石灰石 |
将等质量、等质量分数的氢氧化钠溶液和硫酸溶液混合,混合后的溶液不能与下列物质发生反应的是( )
| A、Ba(OH)2 |
| B、FeCl3 |
| C、HCl |
| D、Na2CO3 |