题目内容
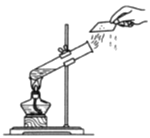
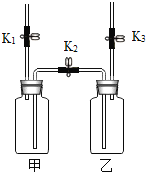
【题目】利用下图的微型装置进行有关实验探究(整套装置气密性良好)。
实验步骤 | 实验现象 |
Ⅰ挤压左边滴管并微热燃烧管 | 红磷和白磷均没有燃烧 |
Ⅱ挤压右边滴管并微热燃烧管 | 红磷没有燃烧,白磷燃烧 |

下列说法不正确的是( )
A.白磷燃烧时,产生白烟,放出热量
B.步骤Ⅱ中,白磷燃烧而红磷不燃烧,说明燃烧需要的条件之一是温度达到可燃物的着火点
C.对比步骤Ⅰ中白磷不燃烧而步骤Ⅱ中白磷燃烧,说明燃烧需要条件之一是可燃物与氧气接触
D.若再次挤压左边滴管,能观察到白磷熄灭,说明二氧化碳不可燃、支持燃烧、且密度比空气大
【答案】D
【解析】
A. 白磷燃烧时,产生白烟,放出热量,说法正确;
B. 白磷的着火点比红磷低,步骤Ⅱ中,白磷燃烧而红磷不燃烧,说明燃烧需要的条件之一是温度达到可燃物的着火点,说法正确;
C. 对比步骤Ⅰ中白磷不燃烧因为没有氧气,而步骤Ⅱ中由氧气,白磷燃烧,说明燃烧需要条件之一是可燃物与氧气接触,说法正确;
D. 若再次挤压左边滴管,能观察到白磷熄灭,说明二氧化碳不能燃烧、也不支持燃烧的性质,但无法说明二氧化碳的密度大,说法错误。
故选:D。

 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案【题目】以下是教材中关于水的一些实验,根据所学水的知识回答下列问题:
|
|
|
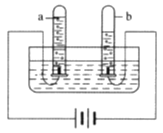
A.水的沸腾 | B.水的电解 | C.水的净化 |
(1)对于实验A中水的沸腾,下列说法正确的是_____(填字母)。
A 水分子之间间隔不变 B 水分子的运动速率加快
C 水分子保持不变 D 保持水化学性质的粒子是氢原子和氧原子
(2)实验B水的电解中试管b得到的气体是_____(填名称)。
(3)实验C中净化水时,小卵石和石英砂的作用是_____。
(4)水是一种重要的化工原料。氯碱工业通过电解饱和氯化钠溶液的方法制取烧碱(NaOH),其中发生的主要反应是氯化钠和水在通电的条件下生成氢氧化钠、氢气、氯气(Cl2),该反应的化学方程式为_____。