题目内容
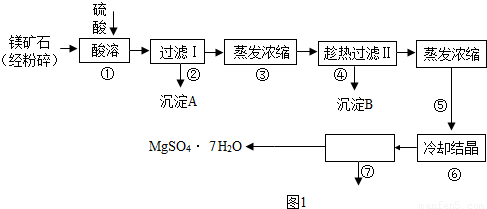
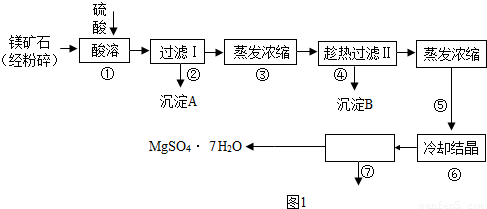
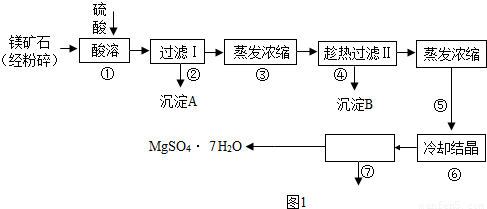
某种镁矿石的主要成分是碳酸镁,还含有较多的脉石(SiO2)和少量石灰石.如图1是利用该镁矿石制备七水硫酸镁(MgSO4?7H2O)的工艺流程: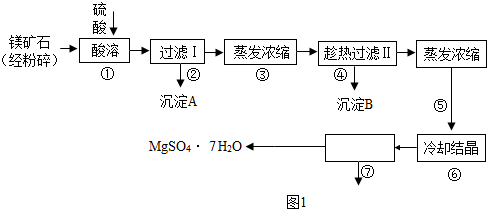
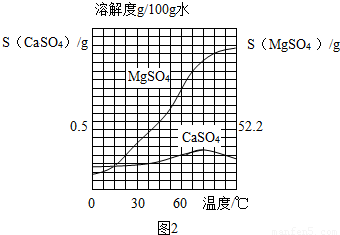
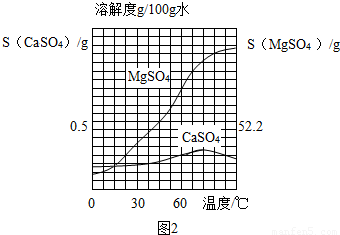
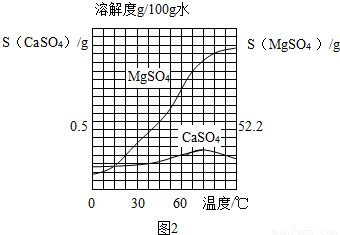
已知CaSO4和MgSO4的溶解度曲线如图2所示: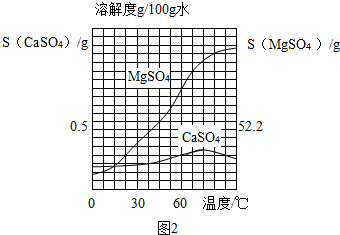
根据以上信息回答下列问题:
(1)写出步骤①中碳酸镁与硫酸发生反应的化学方程式
(2)上述流程中多次用到了过滤操作,实验室过滤时需要用到的玻璃仪器是玻璃棒、烧杯和
(3)沉淀A的成分是SiO2和部分硫酸钙,过滤I后得到的滤液中的溶质除了MgSO4还有
(4)步骤④趁热过滤的作用是
(5)步骤⑦的操作名称是

已知CaSO4和MgSO4的溶解度曲线如图2所示:

根据以上信息回答下列问题:
(1)写出步骤①中碳酸镁与硫酸发生反应的化学方程式
MgCO3+H2SO4═MgSO4+H2O+CO2↑
MgCO3+H2SO4═MgSO4+H2O+CO2↑
.(2)上述流程中多次用到了过滤操作,实验室过滤时需要用到的玻璃仪器是玻璃棒、烧杯和
漏斗
漏斗
.(3)沉淀A的成分是SiO2和部分硫酸钙,过滤I后得到的滤液中的溶质除了MgSO4还有
CaSO4
CaSO4
.(4)步骤④趁热过滤的作用是
MgSO4的溶解度随温度的下降减小较快,趁热过滤可防止因降温导致MgSO4结晶
MgSO4的溶解度随温度的下降减小较快,趁热过滤可防止因降温导致MgSO4结晶
.(5)步骤⑦的操作名称是
过滤
过滤
.分析:(1)根据书写方程式的原则分析
(2)根据过滤用到的仪器分析
(3)根据镁矿石的成分分析
(4)根据硫酸镁和硫酸钙的溶解度分析
(5)根据分离混合物的方法分析
(2)根据过滤用到的仪器分析
(3)根据镁矿石的成分分析
(4)根据硫酸镁和硫酸钙的溶解度分析
(5)根据分离混合物的方法分析
解答:解:(1)碳酸镁和硫酸反应生成硫酸镁、水和二氧化碳,化学方程式为MgCO3+H2SO4═MgSO4+H2O+CO2↑
(2)过滤用到的仪器或用品有铁架台(带铁圈)、烧杯、玻璃棒、漏斗以及滤纸,其中玻璃仪器有烧杯、漏斗、玻璃棒,故答案为:烧杯、漏斗、玻璃棒;
(3)镁矿石的主要成分是碳酸镁,还含有较多的脉石(SiO2)和少量石灰石.加入硫酸后,碳酸镁与硫酸反应生成硫酸镁、水和二氧化碳,碳酸钙和硫酸反应生成硫酸钙、水和二氧化碳,因此过滤后得到的滤液中的溶质除了硫酸镁外还含有硫酸钙.
(4)趁热过滤时,硫酸钙的溶解度较小,而硫酸镁的溶解度较大,易于分离混合物,此时过滤得到的沉淀为CaSO4?2H2O或CaSO4,如不趁热过滤,冷却后硫酸镁的溶解度减小,会生成硫酸镁晶体
(5)步骤⑦是将固体MgSO4?7H2O与水分离,因此要用过滤操作.
故答案为:(1)MgCO3+H2SO4═MgSO4+H2O+CO2↑
(2)漏斗.
(3)CaSO4.
(4)MgSO4的溶解度随温度的下降减小较快,趁热过滤可防止因降温导致MgSO4结晶.
(5)过滤
(2)过滤用到的仪器或用品有铁架台(带铁圈)、烧杯、玻璃棒、漏斗以及滤纸,其中玻璃仪器有烧杯、漏斗、玻璃棒,故答案为:烧杯、漏斗、玻璃棒;
(3)镁矿石的主要成分是碳酸镁,还含有较多的脉石(SiO2)和少量石灰石.加入硫酸后,碳酸镁与硫酸反应生成硫酸镁、水和二氧化碳,碳酸钙和硫酸反应生成硫酸钙、水和二氧化碳,因此过滤后得到的滤液中的溶质除了硫酸镁外还含有硫酸钙.
(4)趁热过滤时,硫酸钙的溶解度较小,而硫酸镁的溶解度较大,易于分离混合物,此时过滤得到的沉淀为CaSO4?2H2O或CaSO4,如不趁热过滤,冷却后硫酸镁的溶解度减小,会生成硫酸镁晶体
(5)步骤⑦是将固体MgSO4?7H2O与水分离,因此要用过滤操作.
故答案为:(1)MgCO3+H2SO4═MgSO4+H2O+CO2↑
(2)漏斗.
(3)CaSO4.
(4)MgSO4的溶解度随温度的下降减小较快,趁热过滤可防止因降温导致MgSO4结晶.
(5)过滤
点评:本题考查了物质的分离与提纯的方法以及酸与盐的化学性质,需学生具体分析问题解决问题的能力

练习册系列答案
相关题目