题目内容
(2010?青岛模拟)节假日里,人们常用色彩斑斓的氢气球点缀喜庆的气氛.填充气球的氢气通常用金属铝和浓氢氧化钠溶液反应制取.(1)某同学对金属铝和浓氢氧化钠溶液反应的化学方程式已配上了部分化学计量数,
请你予以补充完善.2Al+[______]NaOH+2H2O=2NaAlO2+3H2↑
(2)现有18g金属铝,按上面的化学方程式完全反应后可以制取氢气的质量为______g.
【答案】分析:(1)根据反应前后原子种类和个数都不变的特点,配平反应的化学方程式;
(2)利用反应的化学方程式,计算一定质量的金属铝反应后生成氢气的质量.
解答:解:(1)配平时,由于反应部分物质的化学计量数已确定,根据反应前后钠元素的原子个数应相同的,可以判断氢氧化钠化学式的化学计算量,为2;
故答案为:2;
(2)设可以制取氢气的质量为x
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
2×27 6
18g x
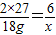
解之得 x=2g
故答案为:2.
点评:配平反应的化学方程式并利用该化学方程式进行相对基础的计算,题侧重基础考查.
(2)利用反应的化学方程式,计算一定质量的金属铝反应后生成氢气的质量.
解答:解:(1)配平时,由于反应部分物质的化学计量数已确定,根据反应前后钠元素的原子个数应相同的,可以判断氢氧化钠化学式的化学计算量,为2;
故答案为:2;
(2)设可以制取氢气的质量为x
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
2×27 6
18g x
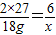
解之得 x=2g
故答案为:2.
点评:配平反应的化学方程式并利用该化学方程式进行相对基础的计算,题侧重基础考查.

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
(2010?青岛模拟)某课外兴趣小组对一批铁样品(含有杂质,杂质不溶于水,也不与稀硫酸反应)进行分析,甲、乙、丙三位同学分别进行实验,其中只有一位同学所取用的稀硫酸与铁样品恰好完全反应.实验数据如下:
请你认真分析数据,回答下列问题:(烧杯的质量为75.4g;计算结果精确到1%)
(1)______同学所取用的稀硫酸与铁样品恰好完全反应;
(2)计算样品中铁的质量分数;
(3)所用稀硫酸的溶质质量分数.
| 甲 | 乙 | 丙 | |
| 烧杯+稀硫酸 | 250g | 200g | 200g |
| 加入的铁样品 | 9g | 9g | 14g |
| 充分反应后,烧杯+剩余物 | 258.7g | 208.7g | 213.7g |
(1)______同学所取用的稀硫酸与铁样品恰好完全反应;
(2)计算样品中铁的质量分数;
(3)所用稀硫酸的溶质质量分数.