题目内容
化学兴趣小组同学在帮助老师整理实验室时,发现了半瓶久置的氢氧化钙粉末,他们决定对这半瓶氢氧化钙粉末的组成进行实验探究。
(1)提出问题:这瓶氢氧化钙是否已经变质?
(2)猜想与假设:该氢氧化钙粉末的成分为①氢氧化钙;②氢氧化钙、碳酸钙;③ 。
(3)设计方案、进行实验:请你参与探究,并填写下表。
|
实验步骤 |
实验现象 |
实验结论 |
|
①取样品少量于小烧杯中,加入适量水,充分搅拌,过滤。 |
|
|
|
② 。 |
大量气泡 产生 |
氢氧化钙已经变质。 |
|
③取少量滤液于试管中, 。 |
|
氢氧化钙没有完全变质。 该反应的化学方程式为 。 |
(4)联想与启示:氢氧化钙变质是由于它与空气中的 发生化学反应的缘故,因此氢氧化钙应 保存。
(2)CaCO3 或碳酸钙 (3)
|
实验步骤 |
实验现象 |
实验结论 |
|
②取少量滤渣与试管中,滴加适量稀盐酸 |
|
|
|
③通入二氧化碳 |
有白色沉淀产生 |
CO2+Ca(OH)2=CaCO3↓+H2O |
(4)二氧化碳 ,密封 (说明:实验方案③的操作和现象共1分,其他每空1分
【解析】(2))氢氧化钙变质后,生成碳酸钙.故有三个可能:①氢氧化钙;②氢氧化钙、碳酸钙;③碳酸钙;故答案为:碳酸钙
(3)氢氧化钙变质后,生成碳酸钙,碳酸钙难溶于水,而氢氧化钙微溶于水.所以我们可以根据是否溶于水,来推断是否变质.根据碳酸钙能与盐酸反应生成二氧化碳气体,然后根据是否有气体产生来判断是否变质生成碳酸钙.根据氢氧化钙与二氧化碳能反应生成沉淀判定粉末中是否还有未变质的氢氧化钙;
(4)氢氧化钙变质是由于Ca(OH)2与空气中的二氧化碳发生化学反应的缘故,因此氢氧化钙应密封 保存

 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
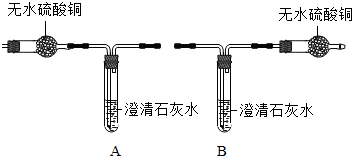
小学同步三练核心密卷系列答案某化学兴趣小组同学发现铜绿[Cu2(OH)2CO3]受热分解后除生成CO2和H2O外,试管中还有一些黑色粉末状固体.
| 小资料:无水硫酸铜为 白色粉末,遇水变蓝. |
(1)若要证明有CO2和 H2O生成,应选择的装置是________(填字母序号);理由是________.
(2)探究黑色粉末的成分.
【猜想与假设】该黑色粉末可能是①碳粉、②氧化铜、③________.
小明同学经过认真分析,认为上述猜想①一定不正确,其理由是________.
【查阅资料】碳粉与氧化铜均为不溶于水的黑色粉末;氧化铜能与稀硫酸反应形成蓝色溶液,碳粉既不与稀硫酸反应也不溶解在稀硫酸中.
【实验验证】请你帮小组同学完成下述实验报告.
| 实验操作与现象 | 实验结论 |
| ________ | 猜想②正确 |
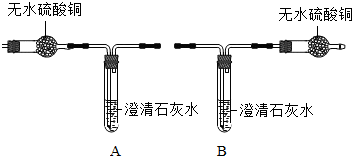
| 小资料:无水硫酸铜为 白色粉末,遇水变蓝. |
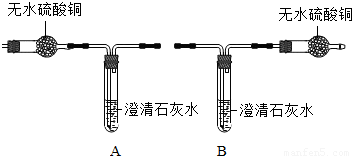
(1)若要证明有CO2和 H2O生成,应选择的装置是______(填字母序号);理由是______.
(2)探究黑色粉末的成分.
【猜想与假设】该黑色粉末可能是①碳粉、②氧化铜、③______.
小明同学经过认真分析,认为上述猜想①一定不正确,其理由是______.
【查阅资料】碳粉与氧化铜均为不溶于水的黑色粉末;氧化铜能与稀硫酸反应形成蓝色溶液,碳粉既不与稀硫酸反应也不溶解在稀硫酸中.
【实验验证】请你帮小组同学完成下述实验报告.
| 实验操作与现象 | 实验结论 |
| ______ | 猜想②正确 |