题目内容
18.“黄铜”是铜锌合金,外观和黄金相似,故称“黄铜”为假黄金,不法商贩用假黄金制成饰品,欺骗消费者.区别真金还是假黄金的方法很多,如取样品放入稀H2SO4中能产生气泡的是假黄金,无现象的是真金,请你再用另一种方法(试剂与上述物质类别不同)区别真金与假黄金(只写出化学方程式)Cu+2AgNO3═Cu(NO3)2+2Ag为了测定该铜锌合金中锌的质量分数,现取铜锌合金样品20.0g,将80.0g稀H2SO4平均分成4等份,分4次加入到样品中,每次充分反应后测得剩余固体质量如表.
| 次数 | 1 | 2 | 3 | 4 |
| 加入稀H2SO4质量(g) | 20.0 | 20.0 | 20.0 | 20.0 |
| 剩余固体质量(g) | 16.75 | 13.5 | 13 | 13 |
(2)20.0g稀硫酸中溶质的质量.(写明计算步骤)
分析 铜能和硝酸银反应生成硝酸铜和银;
锌和稀硫酸反应生成硫酸锌和氢气,1、2次实验次数的氢气质量都是3.25g,3次实验次数的氢气是0.5g,说明第3次实验中锌完全反应,根据产生氢气的质量可以计算锌的质量,教育部可以计算铜锌合金中,锌的质量分数;
根据1次实验可以计算20.0g稀硫酸中溶质的质量.
解答 解:区别真金与假黄金的方法可以是:取样品放入硝酸银溶液中,如果样品表面附着一层银白色物质,说明是假黄金,如果无明显现象,说明是真黄金;
铜和硝酸银反应的化学方程式为:Cu+2AgNO3═Cu(NO3)2+2Ag.
故填:Cu+2AgNO3═Cu(NO3)2+2Ag.
(1)铜的质量是13g,锌的质量分数为:$\frac{20.0g-13g}{20.0g}$×100%=35%,
故填:35%.
(2)设20.0g稀硫酸中溶质的质量为x,
因为1次实验中稀硫酸完全反应,因此以1次实验数据进行计算,
反应的锌的质量为:20.0g-16.75g=3.25g,
Zn+H2SO4═ZnSO4+H2↑,
65 98
3.25g x
$\frac{65}{3.25g}$=$\frac{98}{x}$,
x=4.9g,
答:20.0g稀硫酸中溶质硫酸的质量是4.9g.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,同时考查了分析数据的能力,计算时要注意规范性和准确性.

练习册系列答案
 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
9.化学课上,老师让同学们举一个“缓慢氧化”的例子,大家积极发言,有下列不同的答案,其中不正确的一项是( )
| A. | 动植物的呼吸 | B. | 食物的腐烂 | C. | 酒和醋的酿造 | D. | 蜡烛的燃烧 |
13.NH4NO3、CO(NH2)2、NH4HCO3、NH4Cl都是白色固体,重要的化肥,下列物质能够将尿素从四种物质中鉴别出来的是( )
| A. | 稀盐酸 | B. | 水 | C. | 氯化钠 | D. | 氢氧化钙 |
3.下列物质的应用正确的是( )
| A. |  一氧化碳用于炼钢 | B. |  氮气用于霓虹灯 | ||
| C. |  碳酸氢钠作干粉灭火器 | D. |  氧气用作火箭燃料 |
10.除去下列物质中的杂质(括号内为杂质),所选用试剂及操作均正确的一组是( )
| 选项 | 物质(括号内为杂质) | 所加的试剂 | 除去杂质的方法 |
| A | Na2SO4溶液(NaOH) | 过量的稀硫酸 | 搅拌 |
| B | NaC1(Na2CO3) | 足量的BaC12溶液 | 过滤.蒸发.结晶 |
| C | KC1(KC1O3) | 少量的MnO2 | 加热后冷却 |
| D | H2(CO2) | 足量氢氧化钠溶液和浓硫酸 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
7.正确的化学实验操作对实验结果及人身安全都非常重要.下图所示实验操作中正确的是( )
| A. | 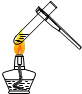 液体加热 | B. | 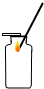 氧气验满 | C. | 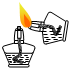 点燃酒精灯 | D. | 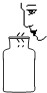 闻气体气味 |
6.一个成年人每分钟大约要吸收8ml氧气,大约需要吸入的空气是( )
| A. | 50 ml | B. | 40ml | C. | 30ml | D. | 20ml |
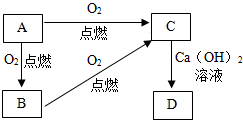 A、B、C、D为初中阶段常见的四种化学物质,它们均含有一种相同的元素.常温下,A为固体单质,B、C、D均为化合物,C是引起温室效应的主要气体.
A、B、C、D为初中阶段常见的四种化学物质,它们均含有一种相同的元素.常温下,A为固体单质,B、C、D均为化合物,C是引起温室效应的主要气体.