题目内容
通过学习,我们知道有多种途径可以制取氧气.如:
A.电解水 B.分离空气 C.加热高锰酸钾 D.分解过氧化氢 E.
(1)相信你在E处还可以写出另一种制取氧气的方法;
(2)若用图1装置加热高锰酸钾制取氧气:
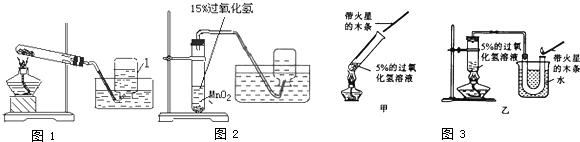
写出标号仪器的名称:① ,实验结束,把导管移出水面,此时发现水槽中的水变成了浅紫红色,你认为产生该现象的原因可能是 ;
(3)若分解过氧化氢制取氧气(如图2),为了探究“过氧化氢的溶质质量分数与分解速率关系”时,用蒸馏水将过氧化氢稀释,取两支大试管分别倒入不同质量分数的过氧化氢,再加入等量的MnO2,各收集一小试管气体,发现浓度大的先收集满.该操作过程中合理的排列顺序是(选填序号) .
①检验装置的气密性;
②待有连续稳定气泡再排水集气;
③将水槽中待收集气体的集气瓶注满水;
④旋紧连有导管的单孔胶塞;
⑤向大试管内倒入适量双氧水再加入少许MnO2粉末.
(4)如图3甲装置做过氧化氢分解实验,带火星的木条很难复燃,设计图乙加U形管,带火星的木条会较易复燃.设计乙装置能使带火星的木条复燃的原因 .
A.电解水 B.分离空气 C.加热高锰酸钾 D.分解过氧化氢 E.
(1)相信你在E处还可以写出另一种制取氧气的方法;
(2)若用图1装置加热高锰酸钾制取氧气:

写出标号仪器的名称:①
(3)若分解过氧化氢制取氧气(如图2),为了探究“过氧化氢的溶质质量分数与分解速率关系”时,用蒸馏水将过氧化氢稀释,取两支大试管分别倒入不同质量分数的过氧化氢,再加入等量的MnO2,各收集一小试管气体,发现浓度大的先收集满.该操作过程中合理的排列顺序是(选填序号)
①检验装置的气密性;
②待有连续稳定气泡再排水集气;
③将水槽中待收集气体的集气瓶注满水;
④旋紧连有导管的单孔胶塞;
⑤向大试管内倒入适量双氧水再加入少许MnO2粉末.
(4)如图3甲装置做过氧化氢分解实验,带火星的木条很难复燃,设计图乙加U形管,带火星的木条会较易复燃.设计乙装置能使带火星的木条复燃的原因
分析:(1)根据制取氧气的方法解答;
(2)根据实验常用仪器的用途和实验注意事项解答;
(3)根据实验室制取氧气的操作步骤解答;
(4)利用氧气能支持燃烧,经常用用带火星的木条复燃来验证是否是氧气;
(2)根据实验常用仪器的用途和实验注意事项解答;
(3)根据实验室制取氧气的操作步骤解答;
(4)利用氧气能支持燃烧,经常用用带火星的木条复燃来验证是否是氧气;
解答:解:
(1)根据制取氧气的常用方法可用加热氯酸钾和二氧化锰,故填加热氯酸钾和二氧化锰;
(2)根据实验室常用仪器的用途是集气瓶,用高锰酸钾制氧气如果高锰酸钾随气流进入导气管和水槽,会使水槽中的水变成浅紫红色,原因可能是高锰酸钾随气流进入导气管和水槽;
(3)根据实验室制取氧气的操作步骤应该是①⑤④③②;
(4)氧气潮湿或不纯很难使带火星的木条复燃,设计乙装置可以使氧气中的水蒸气冷凝,提高了氧气的纯度,故填U形管将氧气中的水蒸气冷凝,提高了氧气的纯度;
答案:
(1)加热氯酸钾和二氧化锰
(2)集气瓶 高锰酸钾随气流进入导气管和水槽
(3)①⑤④③②
(4)U形管将氧气中的水蒸气冷凝,提高了氧气的纯度
(1)根据制取氧气的常用方法可用加热氯酸钾和二氧化锰,故填加热氯酸钾和二氧化锰;
(2)根据实验室常用仪器的用途是集气瓶,用高锰酸钾制氧气如果高锰酸钾随气流进入导气管和水槽,会使水槽中的水变成浅紫红色,原因可能是高锰酸钾随气流进入导气管和水槽;
(3)根据实验室制取氧气的操作步骤应该是①⑤④③②;
(4)氧气潮湿或不纯很难使带火星的木条复燃,设计乙装置可以使氧气中的水蒸气冷凝,提高了氧气的纯度,故填U形管将氧气中的水蒸气冷凝,提高了氧气的纯度;
答案:
(1)加热氯酸钾和二氧化锰
(2)集气瓶 高锰酸钾随气流进入导气管和水槽
(3)①⑤④③②
(4)U形管将氧气中的水蒸气冷凝,提高了氧气的纯度
点评:考点主要考查气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写,综合性比较强.

练习册系列答案
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案
相关题目


 通过学习,我们知道有多种途径可以制取氧气.如:
通过学习,我们知道有多种途径可以制取氧气.如: