题目内容
8.用质量分数为6%的氯化钠溶液(密度为1.04g/cm3),配制100g质量分数为3%的氯化钠溶液.配制过程为:①计算(计算结果保留一位小数):需6%的氯化钠溶液48.1mL,水50.0g.②量取;③在烧杯(仪器名称)中混匀;④装瓶、贴标签.分析 根据溶液配制的步骤以及溶质质量分数公式进行解答.
解答 解:用质量分数为6%的氯化钠溶液(密度为1.04g/cm3),配制100g质量分数为3%的氯化钠溶液.配制过程为:
①计算:设需6%的氯化钠溶液的体积为v,
利用溶液稀释前后溶质质量不变可知:
则v×1.04g/cm3×6%=100g×3%
v=48.1mL
水的质量=100g-48.1mL×1.04g/cm3=50.0g
②量取;③在烧杯中混匀;④装瓶、贴标签.
故答案为:
①48.1;50.0;③烧杯;混匀.
点评 解答本题关键是要知道配制一定质量一定质量分数溶液的基本步骤,需要的仪器,溶质质量的计算,溶剂质量的计算,知道溶液稀释时溶质质量不变.

练习册系列答案
 互动英语系列答案
互动英语系列答案 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案
相关题目
19.化学思想方法是化学实验探究的重要方法,其中之一为控制变量法.如图探究影响反应速率的因素是( )


| A. | 温度 | B. | 盐酸浓度 | C. | 催化剂 | D. | 固体质量 |
16.如图是元素周期表中一格,下列关于铬元素的说法不正确的是( )


| A. | 铬属于金属元素 | B. | 原子核内中子数为26 | ||
| C. | 相对原子质量为52.00 | D. | 原子核外有24个电子 |
13.下列化学方程违背了“客观事实”的是( )
| A. | 2H2O$\frac{\underline{\;\;△\;\;}}{\;}$2H2↑+O2↑ | B. | 2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO | ||
| C. | S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2 | D. | 3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4 |
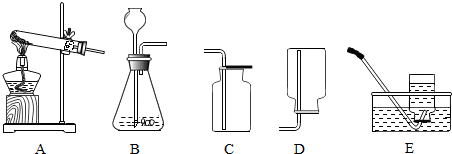
 图1是两种元素在元素周期表中的信息,图2是氯原子的原子结构示意图.
图1是两种元素在元素周期表中的信息,图2是氯原子的原子结构示意图.