题目内容
 某兴趣小组为探究“氧化铁和铜粉”混合物中铜的质量分数,称取一定质量的混合物,按照右图实验装置进行实验:
某兴趣小组为探究“氧化铁和铜粉”混合物中铜的质量分数,称取一定质量的混合物,按照右图实验装置进行实验:(1)实验时要“先通一氧化碳气体,后加热”的目的是
(2)装置A中发生反应的方程式为
(3)实验装置B中的现象是
(4)该装置的设计有一明显不当之处,你的改进方案是
[定量分析]
该兴趣小组按照科学的方案完成实验后,对充分反应后的管内固体X进行如下后续实验探究:

回答下列问题:
(1)写出固体X与稀盐酸反应的方程式:
(2)如何证明固体C已经洗涤干净?
(3)有色溶液B中含有的溶质:
(4)根据以上实验流程,计算原混合物“氧化铁和铜粉”中铜的质量分数为
分析:根据一氧化碳还原氧化铁的步骤、注意事项解答;根据金属与酸反应规律、酸的化学性质及化学方程式进行计算分析解答.
解答:解:(1)一氧化碳具有可燃性,点燃时会可能发生爆炸,实验时要“先通一氧化碳气体,后加热”目的是排尽玻璃管内的空气,防止加热时发生爆炸;
(2)一氧化碳还原氧化铁生成铁和二氧化碳,化学方程式为3CO+Fe2O3
2Fe+3CO2
(3)实验装置B中二氧化碳通入石灰水中,现象是 澄清石灰水变浑浊;发生反应的化学方程式CO2+Ca(OH)2═CaCO3↓+H20
(4)一氧化碳有剧毒,不能直接排放到空气中,故需将尾气点燃或用气球收集起来.
定量分析:(1)反应后管内固体是铁和铜的混合物,加入过量盐酸后,铁与盐酸反应产生氢气,根据氢气的质量可求出铁的质量,根据铁元素的质量可求出氧化铁的质量.反应后溶液中的溶质是铁与盐酸反应生成的氯化亚铁和剩余的盐酸,固体C是铜,表面残留着盐酸,故可取最后的洗涤液滴加紫色石蕊试液,看是否变红确定是否洗涤干净.
故答案为:(1)排尽玻璃管内的空气,防止加热时发生爆炸
(2)3CO+Fe2O3
2Fe+3CO2
(3)石灰水变浑浊CO2+Ca(OH)2═CaCO3↓+H20
(4)将尾气点燃或用气球收集
定量分析:(1)Fe+2HCl═FeCl2+H2↑
(2)取最后的洗涤液滴加紫色石蕊试液,看是否变红,若不变红,说明已洗干净.
(3)FeCl2、HCl.
(4)设铁的质量为x,
Fe+2HCl═FeCl2+H2↑
56 2
x 0.4g
=
x=11.2g
所以氧化铁的质量为
=16g,所以原混合物“氧化铁和铜粉”中铜的质量分数为
×100%=20%
(2)一氧化碳还原氧化铁生成铁和二氧化碳,化学方程式为3CO+Fe2O3
| ||
(3)实验装置B中二氧化碳通入石灰水中,现象是 澄清石灰水变浑浊;发生反应的化学方程式CO2+Ca(OH)2═CaCO3↓+H20
(4)一氧化碳有剧毒,不能直接排放到空气中,故需将尾气点燃或用气球收集起来.
定量分析:(1)反应后管内固体是铁和铜的混合物,加入过量盐酸后,铁与盐酸反应产生氢气,根据氢气的质量可求出铁的质量,根据铁元素的质量可求出氧化铁的质量.反应后溶液中的溶质是铁与盐酸反应生成的氯化亚铁和剩余的盐酸,固体C是铜,表面残留着盐酸,故可取最后的洗涤液滴加紫色石蕊试液,看是否变红确定是否洗涤干净.
故答案为:(1)排尽玻璃管内的空气,防止加热时发生爆炸
(2)3CO+Fe2O3
| ||
(3)石灰水变浑浊CO2+Ca(OH)2═CaCO3↓+H20
(4)将尾气点燃或用气球收集
定量分析:(1)Fe+2HCl═FeCl2+H2↑
(2)取最后的洗涤液滴加紫色石蕊试液,看是否变红,若不变红,说明已洗干净.
(3)FeCl2、HCl.
(4)设铁的质量为x,
Fe+2HCl═FeCl2+H2↑
56 2
x 0.4g
| 56 |
| X |
| 2 |
| 0.4g |
所以氧化铁的质量为
| 11.2g×160 |
| 112 |
| 4g |
| 4g+16g |
点评:化学反应前后元素质量守恒,根据铁元素质量守恒可求出氧化铁质量,进而求出铜的质量分数.

练习册系列答案
相关题目

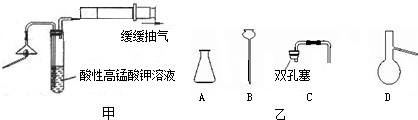
 CO是一种无色、无味、有毒的可燃气体污染物,具有还原性,可用于冶金工业.某兴趣小组为探究其具有还原性,设计了如下实验装置.请回答以下有关问题:
CO是一种无色、无味、有毒的可燃气体污染物,具有还原性,可用于冶金工业.某兴趣小组为探究其具有还原性,设计了如下实验装置.请回答以下有关问题: CO是一种无色、无味、有毒的可燃气体污染物,具有还原性,可用于冶金工业.某兴趣小组为探究其具有还原性,设计了如下实验装置.请回答以下有关问题:
CO是一种无色、无味、有毒的可燃气体污染物,具有还原性,可用于冶金工业.某兴趣小组为探究其具有还原性,设计了如下实验装置.请回答以下有关问题:


