��Ŀ����
�������ƣ�NaNO2����һ�ֹ�ҵԭ�ϣ�������ʳ�������ж������������е�Ԫ�ػ��ϼ���
A. +3 B. -3 C. +1 D. -1
A ��������NaNO2����Ԫ�صĻ��ϼ�Ϊ+1�ۣ���Ԫ�صĻ��ϼ�Ϊ-2�ۣ����ݻ��ϼ۵Ĵ�����ΪŶ����õ�Ԫ�صĻ��ϼ�Ϊ+3�ۣ���ѡA���������ʵ���;�У���Ҫ���������������ʵ���
A�����������и���� B���ɱ����������
C���ƾ�������ȼ�� D����̿����������
�鿴�����в�����������
A. ����ƾ��ƺ�������������
B. ���Ⱥ���Թܣ���������ˮ��ϴ�ɾ�
C. ����ʱ�Թ���Һ������������Թ��ݻ���1��3
D. ʹ���Թܼ����κ��Լ����Թܿڶ�Ӧ��������б
�鿴��ͭ˿�������������ߣ���Ҫ����Ϊͭ����
A. ������ B. ������ C. �ܶȽϴ� D. ����ʴ��
�鿴������Ԫ���������
A. ��������� B. ������ C. ������ D. ����������
�鿴���ؿ��к������Ľ���Ԫ����
A. �� B. �� C. �� D. ��
�鿴�� ��������- ���ͣ���ѡ��
- �Ѷȣ���
 Copyright @ 2008-2013 ����5 ѧϰ�� ManFen5.COM. All Rights Reserved.������
Copyright @ 2008-2013 ����5 ѧϰ�� ManFen5.COM. All Rights Reserved.������
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�ijͬѧ��Һ����ȣ�ʵ�����ʱ����ʹ�õ��Թ������ˣ���ԭ�������
A. �Թܿڶ����Լ�������
B. Һ����������Թ��ݻ���1/3
C. û�в����Թ���ڵ�ˮ�㿪ʼ����
D. ����������ȼ��ȣ��ٹ̶�λ�ü���
C ��������A���Թܶ����˿������ˣ����Dz�������Թ����ѣ����� B��Һ����������Թ��ݻ���1/3�������Һ���⽦������ C��û�в����Թ���ڵ�ˮ�㿪ʼ���Ȼ�ʹ�Թ����Ȳ����ȣ�ը�ѣ���ȷ�� D������������ȼ��ȣ��ٹ̶�λ�ü������Թܼ��ȵ���ȷ����������ѡC�����д����¹ʵķ�������ȷ���ǣ� ��
A�����õ����Ż𩁩���ˮ����
B������ʱ���е��Ͳ����Ż𩁩��ù��Ǹ���
C��������Ȼ���ܵ��Ż𩁩������ر����������Ὺ��ͨ��
D��ɭ���Ż𩁩��ڴ������·��ǰ������ľ����������
�鿴����ͼ �С��͡��𡱷ֱ��ʾ��ͬ��ԭ�ӣ����ܱ�ʾ�������������

A. A B. B C. C D. D
�鿴���ڻ�ѧ�ϣ�����ͬ��Ԫ����ɵIJ�ͬ�ֵ��ʻ���Ϊ��ͬ�������塱�����и������ʲ�����ͬ����������ǣ� ��
A�����Ͱ��� B�����ʯ��ʯī
C�������ͳ�����O3�� D�������������������
�鿴���������ʵĻ�ѧʽ���������������Ķ�Ӧ��ϵ��ȷ����(����)
A. NaOH �ռ� �� B. CO2���� �ɱ� ������
C. NaHCO3 С�մ� �� D. Hg ˮ�� �ǽ���
�鿴�������й�ʵ�������������ȷ����
A. �����ڿ�����ȼ�գ�������������
B. ���ڿ�����ȼ�գ���������������ɫ����
C. ľ̿��������ȼ�ա������⣬���ɶ�����̼
D. ���������о���ȼ�ա��������䣬���ɺ�ɫ����
�鿴�� ��������- ���ͣ���ѡ��
- �Ѷȣ��е�
 Copyright @ 2008-2013 ����5 ѧϰ�� ManFen5.COM. All Rights Reserved.������
Copyright @ 2008-2013 ����5 ѧϰ�� ManFen5.COM. All Rights Reserved.������
�Ȱ�ͪ��C13H16NClO���׳ơ�K�ۡ�����һ������ҩ����ʹ�˲��������ԣ�����˵��������ǣ� ��
A���Ȱ�ͪ���Ƿ�ʹ�ã����Ϊ��Ʒ B���Ȱ�ͪ��32��ԭ�ӹ���
C���������������������ʳ��K���� D���Ȱ�ͪ��̼����Ԫ�ص�������Ϊ39��4
B ��������A���Ȱ�ͪ��һ������ҩ����ʹ�˲��������ԣ������Ƿ�ʹ�ã����Ϊ��Ʒ������ȷ��B���Ȱ�ͪ���ɷ��ӹ��ɵĶ�������ԭ��ֱ�ӹ��ɵģ��ʴ���C���Ȱ�ͪ��һ������ҩ����ʹ�˲��������ԣ����Լ������������������ʳ��K���ۣ�����ȷ��D���Ȱ�ͪ��̼����Ԫ�ص�������Ϊ��12��13������1��16��=39��4������ȷ����ѡB������ͼʾʵ������У���ȷ���� (����)
A.  �ⶨ��Һ��pH B.
�ⶨ��Һ��pH B.  ��������
��������
C.  ��������� D.
��������� D.  ����ʳ��ˮ
����ʳ��ˮ
���б仯�����з�����ѧ�仯���� ( )
A. ����ե֭ B. ����ɻ� C. ��ɴ֯�� D. �����ܽ�
�鿴��ͬѧ��ͨ��ѧϰ������ͭ�Ļ�ѧ���ʽ����˽�һ�����о���
��Ŀһ. ͬѧ�ǽ�����ͭƬ���ھƾ��ƻ��������գ����ֱ����ڣ����ǶԺ�ɫ������Դ��������Ȥ��ͭƬ�����ɫ������ʲô��?
���������ϡ�
��1���ƾ������ȼ�ղ���̿�ڣ������̣���
��2�������Ļ�ѧ���ʱȽϻ��ã������������������ͭ��Ӧ���ɺ�ɫ������ͭ��
��3������ͭ�������ᷴӦ��������ͭ��ˮ��̿��������ˮ���������������Ӧ��
����������衿
����1����ɫ������̿�ڡ�
����2����ɫ�����ǿ����е�������ͭ��Ӧ���ɵ�����ͭ��
����3����ɫ�������̿����������ͭ��
������ʵ�顿
ʵ�鲽��ͷ��� | ʵ������ | ʵ����� |
ʵ��һ��ȡһС�ι���ͭƬ�������Թ��ڣ�Ȼ�����Թܼмг��Թܣ����ھƾ��Ƶ����沿λ���ȡ� | ͭƬ��� | ��1������1����ȷ�� ��2����ɫ�������������е� ______ �йء� |
ʵ�����ȡһ�Թܣ���һС�ι���ͭƬ�����Թ��У����Ͻ���������ע��������Թ��ڵĿ�������ý����������ȣ��۲�������ȡ�½������۲����� | ________ | ����2��ȷ |
ʵ���������ھƾ��ƻ��������պ�ĸ��ź�ɫ�����ͭƬ��Ͷ�뵽ʢ��ϡ������Թ��С� | ________ | ����3����ȷ |
��Ŀ��. ͬѧ��ͨ��ѧϰ֪��ͭ�����ᡢϡ����ܷ�����Ӧ����ȴ���ֻ�ѧ��ʦ��ͭ�������Ʊ�������ȥ������ʵ�顣ͬѧ����ʵ���Ҷ�ͭ��ϡ����ķ�Ӧ������̽����
ʵ��I | |
ʵ��װ�� | ʵ������ |
| ͭƬ����ʧ�� ����ɫ���ݲ������Թ����ϲ��к���ɫ������֣� ��Һ����ɫ��Ϊ��ɫ |
��̽����ʵ��I�в�������ɫ������ʲô?
���������ϡ�
��1�����ᣨHNO3����Cu��Ӧ��������ͭ�ͺ���Ԫ�صĻ��������ͭ��Һ����ɫ��
��2��������NH3������ʹ��̪��Һ���
��3������Ԫ�ص�ijЩ��̬���ʵ���������
NH3 | NO | NO2 | |
��ɫ | ��ɫ | ��ɫ | ����ɫ |
��ζ | �̼��� | �̼��� | |
�ܽ��� | ��������ˮ | ������ˮ | ������ˮ������ |
����������衿��ɫ��������ǣ���NH3 ��NO
������ʵ�顿ͬѧ��������ͼװ�öԲ�������ɫ������м��顣

ʵ����� | ʵ������ |
1. ���ɼУ�ͨ��N2��һ��ʱ��رյ��ɼ� | B��C�е��ܿ�����ɫ����ð�� |
2. ��C�е������뼯��ƿ�У���Һ©���Ļ���������һ����ϡ���ᣬ�رջ��� | A������ɫ���ݲ��� B�е��ܿ�����ɫ����ð�� C�м���ƿ���ռ�����ɫ���� |
3. ��ˮ����ȡ������ƿ���������ڿ����� | ��ɫ�����Ϊ����ɫ |
4. ȡ����B��Һ�����Թ��У��μ���ɫ��̪��Һ | �Թ�����Һ��ɫ�����Ա仯 |
����������ۡ�
��1������1�У�ͨ��N2��Ŀ����__________��
��2��ͬѧ����Ϊ����ٲ���ȷ��������__________��
��3����ɫ������еĻ�ѧ������__________��
�鿴���Ķ�������ն��ġ�
��ɫֲ��Ĺ������
��ԡ�������µ���ɫֲ�������ĵؽ�����һ����Ҫ�Ļ�ѧ�仯����������á�������ɫֲ��ͨ��Ҷ���壬���ù��ܣ��Ѷ�����̼��ˮת���ɴ����������л�����ۣ��������ͷ������Ĺ��̡���ɫֲ��Ĺ��������Ҫʲô������?
��ʵ��1��ʵ��װ������ͼ��ʾ��һ��ʱ���ȡ����ƿ����ס��ҶƬ��δ��ס��һ��ҶƬ���ֱ���ɫ�ȴ������������Һ���۲쵽ǰ���ޱ仯�����߱�����

��С���ϡ�����1������������Ϊ��ɫ��
��2��Ũ����������Һ�ɺͶ�����̼��Ӧ��
��ʵ��2���������裺
����һ��ȡBTB��Һ������ձ��У�����Һ�д�������Һ��ɫ��ơ��ֱ���A��B��C��D�Թ������ӵ�����BTB��Һ������ɫ�����Ѵ�����BTB��Һ��
���������C��D�Թ��и�����һ��ֲ�
������������Ƥ����A��B��C��D 4���Թ�������������ֽ���Թ�D��������4���Թ����ڹ����¡�
�����ģ�һ��ʱ��۲�BTB��Һ�ı�ɫ�����
A�Թ� | B�Թ� | C�Թ� | D�Թ� | |
����һ | BTB��Һ | �Ѵ�����BTB��Һ | �Ѵ�����BTB��Һ | �Ѵ�����BTB��Һ |
����ɫ | ��ɫ | ��ɫ | ��ɫ | |
����� | ����ֲ�� | ����ֲ�� | ||
������ | ���� | ���� | ���� | �ܹ⣨��ֽ������ |
������ | ����ɫ | ��ɫ | ����ɫ | ��ɫ |

��С���ϡ���BTB��������ݷ�����������ݷ�����������Һ���Ա仯����ɫ�����仯�����±�����
���� |
| ||
��ɫ | ��ɫ | ��ɫ���� | ��ɫ |
��ʵ����ɫֲ��Ĺ��������һ���ܸ��ӵĹ��̡�ͨ��������ã�������ת������л��������ת����˻�ѧ�ܣ�ͬʱά�ִ����������Ͷ�����̼��ƽ�⡣
�����������ݣ��ش��������⣺
��1��������õķ�Ӧ����________��
��2��ʵ��1��Ŀ����________��
��3��ʵ��2�У�A��B��C��D 4���Թ�����3�����ʵ�飬������˵�����������Ҫ�ڹ��������½��еĶ���ʵ����________�����Թ���ţ���
��4���������߲��������Ӵ�����Ϊ��ֲ�����߲˵�ũ�����һ�������Ľ��飺________��
�鿴��ij�о���ѧϰС��������ͼװ���о�CO2��NaOH�ķ�Ӧ��
��֪��ˮ�ķе�������ѹǿ�йأ�����ѹǿС���е�ͣ�����ѹǿ�е�ߡ�
ʵ��װ�� | ʵ�鲽�� |
| ��. A�г���CO2��B���ձ��о�ʢ��96�����ϵ�δ���ڵ���ˮ������ʵ�������������ģ��� ��. ��ע������A��ע��һ����ŨNaOH��Һ����۲쵽B����ˮ���ڡ� ��.��ȡ��ͬװ�ã���ע������A��ע��20mLˮ����۲쵽B�е���ˮû�з��ڡ� |
��1�����װ�������ԣ����ϻ�������ע����������һ���߶ȣ����ֺ۲쵽����_________��˵��װ�õ����������á�
��2���������ע��ŨNaOH��Һ�����ӦΪ_________mL��
��3��������Ŀ�����ų�_________�ĸ��š�
��4��ͨ���Ա�_________����֪CO2��NaOHȷʵ�����˷�Ӧ���䷴Ӧ�Ļ�ѧ����ʽΪ_________��
�鿴�� ��������- ���ͣ���ѡ��
- �Ѷȣ��е�
 Copyright @ 2008-2013 ����5 ѧϰ�� ManFen5.COM. All Rights Reserved.������
Copyright @ 2008-2013 ����5 ѧϰ�� ManFen5.COM. All Rights Reserved.������
��ͼʵ��װ�ñ���Ϊ���˹���Ҷ��������C3H8O����Ҫ�Ļ���ԭ�ϣ�Ҳ������ȼ�ϡ�����˵����ȷ����

A. C3H8O�У�̼����Ԫ�ص�������Ϊ3:8
B. ��װ�õ��ܷ�Ӧ���ڻ��Ϸ�Ӧ
C. �˷�Ӧ������3��CO2���ӣ��Ͳ���5��O2����
D. ��װ�ñ���Ϊ���˹���Ҷ������Ҫԭ����ģ����ֲ��Ĺ������
D ��������A. C3H8O�У�̼����Ԫ�ص�ԭ�Ӹ�����Ϊ������3:8����Ԫ�ص������Ȳ�����Ϊ3:8������ B���÷�Ӧ����������C3H8O���������ʲ��ǻ��Ϸ�Ӧ������ C���÷�Ӧ�Ļ�ѧ��Ӧ����ʽΪ6CO2+8H2O 2C3H8O+9O2����3��CO2���ӣ�����4.5��O2���ӣ����� D����װ�ñ���Ϊ���˹���Ҷ������Ҫԭ����ģ����ֲ��Ĺ�����ã���ȷ����ѡD�� ...����ʵ�����һ���ܴﵽʵ��Ŀ�ĵ���
ѡ�� | ʵ��Ŀ�� | ʵ����� |
A | �������� | �������ǵ�ľ����������ƿƿ�� |
B | ����H2��CH4 | �ֱ��ȼ���ڻ����Ϸ���һ�����ձ� |
C | ����CO2�к��е�����CO | �������ȼ |
D | �Ƚ�Zn��Cu��Ag�Ľ������ | ��Zn��Ag�ֱ����CuSO4��Һ�� |
A. A B. B C. C D. D
�鿴����ͼ��ʾװ�ÿ����ڲⶨ�����������ĺ�����ʵ��ǰ�ڼ���ƿ�ڼ�������ˮ�������ϼǺš������йظ�ʵ���˵���У���ȷ����

A. ʵ��ǰҪ���װ�õ�������
B. ����Ϩ���Ӧ���̴��ɼ�
C. ����ƿ��ʣ��������Ǵ����ĵ���
D. ʵ��ʱ��ֻȡ�ü��������ף��ɼ�����Ⱦ�Ҳ�Ӱ��ʵ����
�鿴���ִ�������Դ��������Խ��Խ������ͼʾ�У��������û�������Դ������ǣ�������




A��̫���ܷ��� B���������� C����ϫ�ͺ��緢�� D����������
�鿴�����л�ѧ����ʽ��д��ȷ����
A. S+O2 SO2��
SO2��
B. Cu+2HCl=CuCl2+H2��
C. 2Al+3CuSO4=Al2��SO4��3+3Cu
D. 2Fe+6HCl=2FeCl3+3H2��
�鿴��þ�С���������������������Ԫ�����ڱ��У�þԪ�ص���Ϣ����ͼ��ʾ����ͼ����Ϣ����˵������ȷ����

A. þΪ����Ԫ�� B. ���������Ϊ12
C. Ԫ�ط���ΪMg D. þԭ�ӵ�����Ϊ24.31g
�鿴�� ��������- ���ͣ���ѡ��
- �Ѷȣ��е�
 Copyright @ 2008-2013 ����5 ѧϰ�� ManFen5.COM. All Rights Reserved.������
Copyright @ 2008-2013 ����5 ѧϰ�� ManFen5.COM. All Rights Reserved.������
��ͼ��С��������OK��ʾ���г�����ѧ��Ӧ���ò�ͬ��������ˮ�ķ�����Ҫ����ָ�ϵ����ʷֱ�ͨ��ij�ַ�Ӧ�Ļ�������ֱ������ˮ����ͼ�е�H2O2��O2��������Xһ���������������е�

A. H2 B. H2CO3 C. CH4 D. CuO
C ��������A��������������Ӧ����ˮ�ǻ��Ϸ�Ӧ����ȷ�� B��̼��ֽ����ɶ�����̼��ˮ���ǷֽⷴӦ����ȷ�� C��������������Ӧ���ɶ�����̼��ˮ���÷�Ӧ���ǻ�����Ӧ���ͣ����� D������ͭ��������Ӧ����ˮ��ͭ�����û���Ӧ���ǻ�����Ӧ���ͣ���ȷ����ѡC�����л�ѧ���ű�ʾ��ȷ����
A. ������ FeO B. 2����ԭ�� H2
C. ������ Ca+2 D. �����K2MnO4
�鿴������ʾ��ͼ��ʾ��������Ҫ�ɷ֣���֪��ͬ��ͬѹ�£���������֮�ȵ��ڷ��Ӹ���֮�ȣ�����ͼ�����������

A B C D
A. A B. B C. C D. D
�鿴���ڼ�ѹ�����£�40 m3��ʯ��������װ��0.04 m3�ĸ�ƿ�У���˵��
A. ����֮���м�� B. ������ԭ�ӹ���
C. ���ӵ�������С D. �����ڲ��ϵ��˶�
�鿴�����й��ڼ�ȩ��CH2O����˵���У���ȷ����
A. ��ȩ��4��ԭ�ӹ���
B. 1����ȩ�����к���1��ˮ����
C. ��ȩ��̼����Ԫ��������Ϊ1:2
D. ��ȩ������Ԫ�����
�鿴���������ƣ�NaNO2����һ�ֹ�ҵԭ�ϣ�������ʳ�������ж������������е�Ԫ�ػ��ϼ���
A. +3 B. -3 C. +1 D. -1
�鿴�� ��������- ���ͣ���ѡ��
- �Ѷȣ��е�
 Copyright @ 2008-2013 ����5 ѧϰ�� ManFen5.COM. All Rights Reserved.������
Copyright @ 2008-2013 ����5 ѧϰ�� ManFen5.COM. All Rights Reserved.������
�ؿ��к������Ľ���Ԫ����
A. �� B. �� C. �� D. ��
A ���������ؿ���Ԫ�غ���ǰ��λ��˳��Ϊ�����衢���������ʺ������Ľ���Ԫ����������ѡA����ѧ��ȤС���ijƷ��������̼��ƺ�����������̽����������Ħ������Ҫ��̼��ơ�����������ɣ������ɷ���������ʱ���������ɡ���������ͼ��ʾװ�ã�ͼ�мг�������ȥ������ʵ�飬��ַ�Ӧ�ⶨB�����ɵ�BaCO3������������ȷ��̼��Ƶ�������������ش��������⡣����֪����ʯ�ҹ������Ҫ�ɷ�����ʯ�Һ��ռ
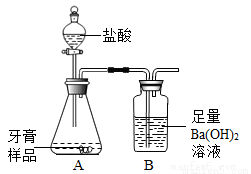
��1��װ��A��������Ʒ������_______�����������ƣ��У����������װ��______�����������ƣ��У�A�����ٷ���___�������֣�����Ӧ��д������һ����Ӧ�Ļ�ѧ����ʽ______
��2�����ⶨֵ��ʵ��ֵС�����ܵ�ԭ����________________������ĸ��
a��װ��A��ˮ������HCl�Ƚ���װ��B��
b��װ��A��CO2δ��ȫ����װ��B
c��CO2�����ٶ�̫�쵼��Ba(OH)2δ��ȫ����
d������δ�μӹ���
��3��Ϊ�������ֲ�ȡ����һЩ��ʩ��
����A��B֮������һ��װ��_____���ѧʽ����Һ��ϴ��ƿ������������___��
������װ��B�еij������·�����һ��������ݣ�������___��
������װ��A��ǰ��������һ�����뵪����װ�ã�Ŀ����_____________��
������װ��B�ĺ���������һ��װ�м�ʯ�ҹ���ĸ���ܣ�Ŀ����___________________
��4��ȷ��ȡ���ݸ�16.00g����Ʒ�����вⶨ�����BaCO3�����ֱ�Ϊ3.96g��3.92g��3.94g���������Ʒ��̼��Ƶ�������������д��������̣�_______
��5��ijͬѧ�������������ⶨ�����и�Ԫ�ص�����������С��ͬѧ��Ϊ��ʹ��ʹ�ų�ʵ�������Ͳ�����Ӱ�죬�����ⶨ�Ľ�����п���ƫС�������ǣ�
_______��
�鿴����±ʯ��K2SO4��MgSO4��2 CaSO4��2H2O�����ڡ�����Ϊ�ܳ�����ü���Դ���ñ��͵�Ca(OH)2��Һ����±ʯ�Ʊ�����أ������������£�
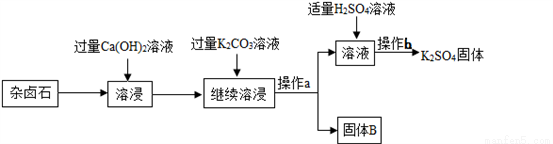
��֪��
���� | CaSO4 | K2SO4 | Mg��OH��2 |
�ܽ��/g(25��) | 0.28 | 11.1 | 0.00084 |
��1������a������Ϊ________���ò����в�������������___________��
��2������B����Ҫ�ɷ���________��________��
��3������b�IJ���������Ũ����________�����ˡ�ϴ�ӡ�
��4����ʵ�������м��������K2CO3��Һ���ܳ�ȥ��������______________��
��5����ʹ��Ca(OH) 2��Һ��K2CO3��Һ����±ʯ���С��ܽ���ʱ��Ϊ̽����ýϸ߽�����±ʯ��Ҫ�ɷֵĽ�ȡ�ʣ�ijʵ��С���ò�ý�ȡҺ��K+��������������ʾ��ȡ�ʣ�����ͬ��ʱ������������ʵ���飺
ʵ�� | �¶�/�� | Ca��OH��2����/g | K+��ȡ��/% |
�� | 25 | 2.5 | 72.4 |
�� | 40 | 2.5 | 86.55 |
�� | 40 | 3 | 90.02 |
�� | 60 | 3 | 91.98 |
�� | 60 | 4 | 91.45 |
������ʵ��������У��¶���K+��ȡ�ʵĹ�ϵ��_______________
��������г���5��ʵ���У���Ҫ�����ѵ�K+��ȡ�ʣ�ѡ��ķ�Ӧ������________���_____________g ��Ca(OH)2����
�鿴����ʮ��������ѧ�����߶�̼����������⻯�����˹㷺������о���ȡ����һЩ��Ҫ�ɹ���
��1����ҵ�ϳ����ý�ˮ�����絽���ȵ�̿����ʵ��ú���������Ƶ�CO��H2�����÷�Ӧ�Ļ�ѧ����ʽ��_______���Ƶõ�CO��һ���ж����壬�ܽ���_________��Я��������
��2������ú��������������̿�㽻�����������ˮ���������������Ŀ����________�������õ���������ڼ��Ⱥʹ����ºϳ�Һ��ȼ�ϼ״�CH3OH���÷�Ӧ����ʽΪ
________________________________________��
��3����ѧ���õ����ز�����ͭ��װ��ͼ���˹����ϵͳ�����ø�װ�óɹ���ʵ������CO2��H2O�ϳ�CH4��
��д���ϳɼ���Ļ�ѧ����ʽ_________��
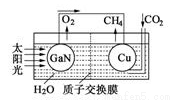
��Ϊ��߸��˹����ϵͳ�Ĺ���Ч�ʣ�����װ���м���������_______��ѡ��������ơ������ᡱ����
�鿴�����꣬�й������ѽ�������ę́���������ݳ�Ʒ���У�ę́�Ƽ۸�һ�����ǣ�һƿ����

����˵�����dzµ��㡱���ŵ���ζ˵��______����50ml�ľƾ���50ml��ˮ������С��100ml����������______��
�� ������Ҫ�õ���������ˮ�Գ�ȥ�����Σ�����______������ˮ��Ӳˮ�������г���______�İ취��Ӳˮת��Ϊ��ˮ��
������Ҫ�õ���������ˮ�Գ�ȥ�����Σ�����______������ˮ��Ӳˮ�������г���______�İ취��Ӳˮת��Ϊ��ˮ��
��Ŀǰ�ҹ��Ѿ���ʼ�ƹ�ʹ���Ҵ����ͣ��Ҵ���������_________ �������������� 
 ��д���Ҵ�����ѧʽC2H6O����ȫȼ�յĻ�ѧ����ʽ_______________________��
��д���Ҵ�����ѧʽC2H6O����ȫȼ�յĻ�ѧ����ʽ_______________________��
�ܿ�ѧ�о����֣����������к����档�ƾ�������Դ����ڵ������׳��¹ʡ��ƺ��ʻ��һ��Υ����Ϊ������ͨ���ƾ��������ʾ����ɫ�仯���ɿ��ٲ��˾���Ƿ�ƺ�ݳ����䷴Ӧԭ��Ϊ��2CrO3(��ɫ)+3C2H5OH+3H2SO4 = Cr2(SO4)3(��ɫ)+3CH3CHO+6X������X�Ļ�ѧʽΪ____________��
�鿴����1����������ͭ�����������г����Ľ�����
������������Ʒ�У���Ҫ���ý����������õ����Ե���___________ �����)
�����) 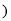 ��
��
A. ���� B��
���� B�� �ֵ��� C��
�ֵ��� C�� ����������
����������
�������кܺõĿ���ʴ���ܣ�ԭ����_______(�û�ѧ����ʽ��ʾ)��
���ڸ����£����ý�̿��������Ӧ���ɵ�һ����̼�ɰ���������ʯ�ﻹԭ���������н�̿�������ǣ��ṩ������____________����¯�����������������������ĺ�̼��Ϊ________��
�ܼ�������δϴ�����ɣ�����һ��ʱ�����ֺ��ɫ��ߣ�����Ҫ��ԭ��������________��_________�Ӵ�����������ʴ��д��������Ԥ����������ķ�����_________��
��2�������һ�ִ���ϲ����ʳ�ģ����е����ʡ�ά����A��ά����C����ά�ء����������Ǻͷḻ������п���Ƶ�Ԫ�أ����У�

����������������Ԫ�ص���_________��ȱ_________���¹������ɡ�
������������а��������ǡ�_________����������_________������ڡ������ڡ����л��߷��ӻ����
�۵����������������յ�ˮ�����Ϊ�����ᣬд����������һ�ָ��������ʵ�����________��
�鿴�� ��������- ���ͣ���ѡ��
- �Ѷȣ���
 Copyright @ 2008-2013 ����5 ѧϰ�� ManFen5.COM. All Rights Reserved.������
Copyright @ 2008-2013 ����5 ѧϰ�� ManFen5.COM. All Rights Reserved.������
��֪A��B��C��D�����ֲ�ͬ��������ʣ���������ͼ��ת����ϵ(�������ʺͷ�Ӧ������ȥ)��A���������ߵĽ�����B����Ԫ��ռ30%��D��ˮ��Һ����ɫ������������ũҩ������Һ������A��__________��B��A�Ļ�ѧ����ʽΪ_________________��C��D�Ļ�ѧ����ʽΪ____________________________________��
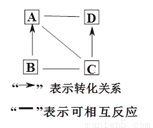
������ͼ�ס����������ʵ��ܽ�����ش�������⣺
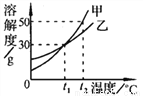
(1)��______��ʱ���ס��ҵ��ܽ����ͬ��
(2)t2��ʱ������75 g�ı�����Һϡ�ͳ�10 %�����ˮ������Ϊ________g��
(3)��t2��ʱ���ס����������ʵı�����Һ������t1��(������������)��������Һ���������������Ĺ�ϵ�Ǽ�_________(�����������������)�ҡ�
�鿴����ͼ��ij��Ӧ����ʾ��ͼ���÷�Ӧ����Է���������С��������_________����Ӧ�Ļ�ѧ����ʽΪ___________���μӷ�Ӧ�ļ��ҵ��������������Ϊ___________��
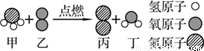
���÷��ӵ����֪ʶ���ͣ� һ��ˮ��Լ����1.67��1021��ˮ����______________��������Ķ��������______________________________________��
�鿴����Na��C��H��O��ѡ��Ԫ����ɷ���Ҫ������ʣ����仯ѧʽд������һ����________�������Ҵ���ѧ���ʵ���_________________��
�鿴����һ��������CO��CO2�Ļ������ͨ�������ij���ʯ��ˮ�У���ַ�Ӧ�����ɳ���������ǡ�õ���ԭ����������������ԭ���������CO��CO2��������Ϊ
A. 7��11 B. 11��14 C. 14��11 D. 11��7
�鿴�� ��������- ���ͣ��ƶ���
- �Ѷȣ���
 Copyright @ 2008-2013 ����5 ѧϰ�� ManFen5.COM. All Rights Reserved.������
Copyright @ 2008-2013 ����5 ѧϰ�� ManFen5.COM. All Rights Reserved.������
�ճ���ʳӦע�������䡣����ʳ���и���ά���ص���
A. �������� B. ���⡢���� C. ˮ�����߲� D. ����ֲ����
C ��������A�����������и������࣬�ʴ���B������ͼ����и��������ʣ��ʴ���C��ˮ�����߲��и���ά���أ�����ȷ��D����ֲ�����и�����֬���ʴ���ѡC�����������г����ı仯���������仯����
A. ������� B. ľ̿ȼ�� C. ʳ�︯�� D. ��ѩ�ڻ�
�鿴��1860�꣬Ӣ����ѧ�ҷ�������Ϊ�����ͯ�����Ļ�ѧ������������Ͳ�����������һ��ʮ����Ȥ�ġ���ĸ���桱ʵ�飬��ͼ��

�������������ܵ�һ�˲����������(ĸ����)�����IJ�λ��ȼ�ŵĻ����ڵ�����һ�˵ļ��촦�����ּ��촦Ҳ�����˻���(�ӻ���)��
������ʪ���ë����ס���ܣ������ӻ���Ϩ��
�����µ���ȥ��ë�������ֵ����ڱڸ��������Ĺ��塣
���������ʵ������е����ش��������⣺
(1)����Ϊ�����������Ĺ������Ҫ�ɷ�Ӧ����_______��
(2)�ӻ����еĿ�ȼ����______________�������ܲ�����ĸ������һ��������ʯ�������ʾ����ģ����У���ѧ������_______________________������������____________________________��
(3)��ʵ��ɹ��Ĺؼ������㣺һ������ʵ��ʱ�������ܲ��˹����������ܲ����ӻ��棬��ԭ����______________�����ǵ����ܱ�����뵽ĸ��������Ĵ������Dz嵽������Ҳ���ܲ����ӻ��棬��ԭ����_________________________��
(4)��������Ϊ________�㣬�¶���ߵ���__________��
�鿴�������ǻ�ѧʵ���г����Ļ�����������ͼ�ش��������⣺

(1)��ͼ����ʾ������ϸ��ƿ�㵹Һ��ʱ��ϸ��ƿ��ǩ��һ��Ҫ_____________��ƿ��__________���������ϡ�
(2)��ͼ����ʾ������ƾ��ƺ����õ�ñ���𡢸��������һ�µ�ñ�������¸Ǻá�����ԭ�����������ȷ��һ����_______(�����)��
A��ƽ����ѹ������ȡ�µ�ñ
B���ӷ�ˮ�֣����ڵ�ȼ�ƾ���
C�����ٻӷ������ڽ�Լ�ƾ�
(3)��ͼ����ʾ������Թ��ڱڸ��в���ϴ��������ʱ����ϴ�Թ�һ�������Թ�ˢպȥ�۷�_______����������ˮ��ϴ������ˮ��ϴ��Ȼ�����Թܼ������ɡ�
�鿴����ѧʵ���ǽ��п�ѧ̽������Ҫ��ʽ��������ѧʵ�鼼����ѧϰ��ѧ�ͽ���̽����Ļ����ͱ�֤����Ҫ��ش��������⣺
(1)����д����ѧ�������Ƽ���Ҫ��;��

д���٢ڢ۵����ƣ�
��___________����___________����___________��
д���ܢ���Ҫ��;��
��___________________________________��____________________________________��
(2)����д��ʵ�����ע�����
��ʵ������Ϩ��ƾ��ƻ���ʱ��Ӧ����_______����
����ʵ������Щ���������Dz��ܱ����ȵģ���_______(��һ��)��
����ʵ����������Ͳ��ȡҺ�����ʱ������Ҫ______________________________________��
����ʵ�������㵹Һ��ҩƷʱ��Ӧʹ��ǩ�������ģ�������ܵ���________��
�鿴�����ݻ�ѧʵ��������������ʵ���������գ�
(1)��ƾ��������Ӿƾ������ɳ����ƾ����ݻ���_______��
(2)���Թ����Һ����ȣ�Ӧʹ���ԹܼУ��������Թܿڴ�Լ_______�����Թ����Һ������������Թ��ݻ���_______���Թܿ�б���ϣ����������_______�ǣ��Թܿڲ�Ҫ�����Լ������ˡ�
(3)ȡ��Һ��ҩƷʱ����û��˵��������һ��ȡ_______��
�鿴�� ��������- ���ͣ���ѡ��
- �Ѷȣ���
 Copyright @ 2008-2013 ����5 ѧϰ�� ManFen5.COM. All Rights Reserved.������
Copyright @ 2008-2013 ����5 ѧϰ�� ManFen5.COM. All Rights Reserved.������
(1)����ֻ֤��������̼�ܶȴ��ڿ�����ͼ��________________________
(2)��ͼ��ʾ�ǡ�����������ͭ��Һ��Ӧǰ�������IJⶨ����ʵ��,��ش���������:
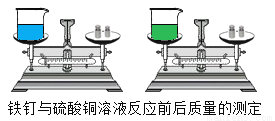
��д������������ͭ��Һ��Ӧ�Ļ�ѧ����ʽ,������ʵ������__________________
�ڸ�ʵ���ܷ���֤�����غ㶨��?__________________
Fe+CuSO4=Cu+FeSO4���������к�ɫ�������ɣ���Һ����ɫ���dz��ɫ( ��,���Ǹ���ѧ��Ӧ,��Ӧǰ��������� ��������(1)֤��������̼�ܶȴ��ڿ�����ͼΪ���� ��2�����������Ļ�Ա�ͭǿ�������������û�������ͭ�е�ͭ�������������ı��棬��Һ���Ϊ����������dz��ɫ��Һ����ѧ����ʽΪ��Fe+CuSO4�TCu+FeSO4���ڷ���ʵ��ԭ����ʵ�������֪������������ͭ��Һ��Ӧǰ������...���û�ѧ����ʽ��ʾ���з�Ӧԭ����
(1)�Ҵ�(��ѧʽΪC2H5oH)����ȼ�ϡ�________________________
(2)���ʳ��ˮ�ɵõ��ռ������������________________________
�鿴����һ����ɫ��ĩ�����ܺ���̼��ơ�̼���ƺ����������е�һ�ֻ��֣�ijѧ��Ϊ��ȷ������ɣ�������ʵ�飬���������ʵ����������ƶϣ�
��1�����Թ��м���������ĩ��ע������������ˮ������õ���ɫ����Һ��
��2��ȡ��1����������Һ������ϡ���ᣬ�����ݲ�����
��3��ȡ��1����������Һ������ʯ���Һ����ɫ��
��ð�ɫ��ĩһ������________�����ܺ���________��
�鿴����Cu(NO3)2��Mg(NO3)���Ļ����Һ�м���һ���������ۣ���ַ�Ӧ����ˡ����˳��������ϵμ�ϡ����ʱ�����ݲ�������Ӧ������������һ������ ����Ӧ��������Һ��һ������ ���йصĻ�ѧ��Ӧ����ʽΪ ����дһ�����ɣ�
�鿴����ͼ��ij�������ʵ��ܽ�����ߡ�
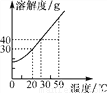
(1)30 ��ʱ�������ʵ��ܽ��Ϊ________g��
(2)50 ��ʱ����40 g�����ʼ��뵽100 gˮ�У������õ�����________(������ͻ����͡�)��Һ��������Һ���µ�20 ��ʱ����������________g��
�鿴��(1)Ӳˮ�к��н϶��Mg2+��________,�����չ����кܶ�ˮ��,��ˮ���Ļ�ѧ����ʽ��______________________(д��һ������)
(2)ʳ��ˮ�к�������CaCl2��Na2SO4,���μ��������BaCl2��Na2CO3��Һ�����,��Һ�е�����Ϊ___________��ʳ��ˮ��ͨNH3��CO2,���Ƶ�С�մ��һ�����,�õ��ʵĻ�ѧʽΪ______________��
�鿴�� ��������- ���ͣ��ۺ���
- �Ѷȣ��е�
 Copyright @ 2008-2013 ����5 ѧϰ�� ManFen5.COM. All Rights Reserved.������
Copyright @ 2008-2013 ����5 ѧϰ�� ManFen5.COM. All Rights Reserved.������



 ��ǿ
��ǿ ]
]