题目内容
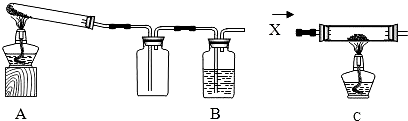
某课外活动小组的同学利用下列实验装置制取气体,请回答下列问题:
(1)图中a、b仪器的名称:a______,b______.
(2)小红用装置A制取氧气,反应的化学方程式是______ K2MnO4+MnO2+O2↑
【答案】分析:(1)熟悉常见仪器,了解名称,根据装置图辨识常见仪器并写出正确的仪器名称;
(2)实验室制取气体的发生装置的选择依据是反应物的状态和反应的条件,从图看试管口处有棉花团可断定是用高锰酸钾制氧气,用高锰酸钾制氧气的反应原理为2KMnO4 K2MnO4+MnO2+O2↑,是加热固体的反应;根据装置B的使用特点是固体与液体不需要加热,判断应用该装置制取氧气时所需要的药品,固体药品二氧化锰是反应的催化剂;
K2MnO4+MnO2+O2↑,是加热固体的反应;根据装置B的使用特点是固体与液体不需要加热,判断应用该装置制取氧气时所需要的药品,固体药品二氧化锰是反应的催化剂;
(3)根据BDE装置的特点,结合二氧化碳的性质来完成该题前两个空的解答,C装置是一种类似于启普发生器的装置,故可以参照启普发生器的优点来解答该题.
解答:解:(1)图中a是酒精灯,b是长颈漏斗.故答案为:酒精灯;长颈漏斗.
(2)图A是加热固体制取气体的反应装置,且在试管口处有一团棉花,故小红是加热高锰酸钾制取氧气,此反应的反应物是高锰酸钾,生成物是锰酸钾、二氧化锰和氧气.图B装置是固液在常温下制取气体的发生装置,在实验室中常用双氧水和二氧化锰制取氧气,其中二氧化锰是反应的催化剂,起催化作用,加快反应的进行.故答案为:2KMnO4 K2MnO4+MnO2+O2↑;催化作用
K2MnO4+MnO2+O2↑;催化作用
(3)二氧化碳是酸性气体,所以应该选择浓硫酸来干燥,故在D装置中应该加入浓硫酸,又由于D装置是干燥装置,气体应从d管进,若从e管进的话,气体将会把浓硫酸压出,由于二氧化碳的密度比空气的大,所以在用E装置来收集二氧化碳时,应该从f管进入;C装置是一种类似于启普发生器的装置,所以其优点是可以随时控制反应的发生和停止.故答案为:浓硫酸;c d e f;可以随时控制反应的发生和停止
点评:本题主要考查了实验室制取气体的装置,要解决好此类题目,要熟记常用气体的发生装置和收集装置的选取方法及其依据,并根据气体的制取原理来组装、选配、判断或者选择气体的发生装置;再根据气体的溶解性、密度及其是否与水或者空气发生反应等来判断、选用收集装置.
(2)实验室制取气体的发生装置的选择依据是反应物的状态和反应的条件,从图看试管口处有棉花团可断定是用高锰酸钾制氧气,用高锰酸钾制氧气的反应原理为2KMnO4
 K2MnO4+MnO2+O2↑,是加热固体的反应;根据装置B的使用特点是固体与液体不需要加热,判断应用该装置制取氧气时所需要的药品,固体药品二氧化锰是反应的催化剂;
K2MnO4+MnO2+O2↑,是加热固体的反应;根据装置B的使用特点是固体与液体不需要加热,判断应用该装置制取氧气时所需要的药品,固体药品二氧化锰是反应的催化剂;(3)根据BDE装置的特点,结合二氧化碳的性质来完成该题前两个空的解答,C装置是一种类似于启普发生器的装置,故可以参照启普发生器的优点来解答该题.
解答:解:(1)图中a是酒精灯,b是长颈漏斗.故答案为:酒精灯;长颈漏斗.
(2)图A是加热固体制取气体的反应装置,且在试管口处有一团棉花,故小红是加热高锰酸钾制取氧气,此反应的反应物是高锰酸钾,生成物是锰酸钾、二氧化锰和氧气.图B装置是固液在常温下制取气体的发生装置,在实验室中常用双氧水和二氧化锰制取氧气,其中二氧化锰是反应的催化剂,起催化作用,加快反应的进行.故答案为:2KMnO4
 K2MnO4+MnO2+O2↑;催化作用
K2MnO4+MnO2+O2↑;催化作用(3)二氧化碳是酸性气体,所以应该选择浓硫酸来干燥,故在D装置中应该加入浓硫酸,又由于D装置是干燥装置,气体应从d管进,若从e管进的话,气体将会把浓硫酸压出,由于二氧化碳的密度比空气的大,所以在用E装置来收集二氧化碳时,应该从f管进入;C装置是一种类似于启普发生器的装置,所以其优点是可以随时控制反应的发生和停止.故答案为:浓硫酸;c d e f;可以随时控制反应的发生和停止
点评:本题主要考查了实验室制取气体的装置,要解决好此类题目,要熟记常用气体的发生装置和收集装置的选取方法及其依据,并根据气体的制取原理来组装、选配、判断或者选择气体的发生装置;再根据气体的溶解性、密度及其是否与水或者空气发生反应等来判断、选用收集装置.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
某课外活动小组的同学将过量的炭粉和16克氧化铜均匀混合,用下图所示装置进行实验.图中铁架台等装置已略去.请回答有关问题:
(1)同学们想通过测定消耗碳、氧元素的质量和生成二氧化碳的质量,分析氧化铜和炭粉反应产生的气体除CO2外是否还有其它产物.反应一段时间后停止加热,冷却到室温.反应前、后测得的数据如下:
分析数据发现,反应中消耗碳和氧元素的质量 (填“大于”、“小于”或“等于”)生成二氧化碳的质量.下列4项中跟这一结果有关的有哪几项? .(填写字母)
A.装置中还有一部分CO2未被石灰水溶液吸收
B.氧化铜和炭粉反应产生的气体除CO2外还有CO
C.氧化铜和炭粉没有完全反应
D.该反应不符合质量守恒定律
(2)有同学认为用图示装置C代替上面的装置A,加热前先通一会气体X,停止加热后再通一会该气体,这样可使实验测得的数据更能准确的说明问题.你认为在O2、N2和H2三种气体中,X应选择哪一种气体? .
(3)实验中最多能得到铜多少克?(写出计算过程)

(1)同学们想通过测定消耗碳、氧元素的质量和生成二氧化碳的质量,分析氧化铜和炭粉反应产生的气体除CO2外是否还有其它产物.反应一段时间后停止加热,冷却到室温.反应前、后测得的数据如下:
| 装置 | 反应前 | 反应后 |
| A | 试管的质量38.2 克 氧化铜和炭粉混合物的质量20.0克 |
试管和固体物质的质量56.8 克 |
| B | 反应后瓶内石灰水比反应前增重1.1 克 | |
A.装置中还有一部分CO2未被石灰水溶液吸收
B.氧化铜和炭粉反应产生的气体除CO2外还有CO
C.氧化铜和炭粉没有完全反应
D.该反应不符合质量守恒定律
(2)有同学认为用图示装置C代替上面的装置A,加热前先通一会气体X,停止加热后再通一会该气体,这样可使实验测得的数据更能准确的说明问题.你认为在O2、N2和H2三种气体中,X应选择哪一种气体?
(3)实验中最多能得到铜多少克?(写出计算过程)

 (2012?海珠区一模)某课外活动小组的同学为测定一瓶BaCl2溶液溶质的质量分数,做了以下实验,请回答有关问题:
(2012?海珠区一模)某课外活动小组的同学为测定一瓶BaCl2溶液溶质的质量分数,做了以下实验,请回答有关问题: