题目内容
4.如图是A、B、C三种不含结晶水的固体物质的溶解度曲线,下列说法中正确的是A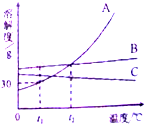
A、t1℃时,65gA的饱和溶液中含有50g溶剂,但将30克B加入到100克水中会形成B的不饱和溶液
B、在t2℃,A、B两种饱和溶液溶质质量分数相同,所含溶质的质量也相等
C、将t1℃A、B、C三种物质的饱和溶液升温至t2℃时,溶液中溶质质量分数由小到大的顺序为C<B=A
D、当A中含有少量B时,提纯A的方法是冷却热饱和溶液(或降温结晶).
分析 A、据此温度下AB的溶解度大小分析解答;
B、不知饱和溶液的质量是否相等,无法判断两溶液所含溶质是否相等;
C、据饱和溶液中溶质的质量分数计算方法及物质的溶解度随温度变化情况分析解答;
D、据AB溶解度受温度影响情况分析提纯物质的方法.
解答 解:A、t1℃时A的溶解度是30g,即100g水中最多溶解30g的A,65gA的饱和溶液中含有50g溶剂,而B的溶解度大于A,所以将30克B加入到100克水中不会形成B的饱和溶液,正确;
B、不知饱和溶液的质量是否相等,无法判断两溶液所含溶质是否相等,故错误;
C、t1℃A、B、C三种物质的饱和溶液升温至t2℃时,AB的溶解度增大,溶液中溶质、溶剂的质量不变,溶质的质量分数不变,与升温前相等,而C的溶解度减小,析出晶体,溶质的质量分数减小;饱和溶液中溶质质量分数的计算式$\frac{溶解度}{溶解度+100g}$×100%,可知溶解度大则溶质的质量分数大,t1℃B的溶解度大于t2℃时C的溶解度大于t1℃A的溶解度,所以溶液中溶质质量分数由小到大的顺序为A<C<B,故错误;
D、A的溶解度受温度影响较大,B的溶解度受温度影响较小,所以当A中含有少量B时,可用冷却热饱和溶液或降温结晶的方法提纯A;
故答案为:A;D:冷却热饱和溶液(或降温结晶).
点评 明确溶解度概念、溶解度曲线的意义、饱和溶液中溶解度大则溶质的质量分数大等知识,即可结合题意灵活解答相关问题.

练习册系列答案
 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案
相关题目
9.最近科学家研制出一种能抗击埃博拉病毒的药物,其化学式为C5H4N3O2F,有关说法正确的是( )
| A. | 每个分子中含有1个氧分子 | B. | 碳、氢元素的质量比是5:4 | ||
| C. | 每个分子由15个原子构成 | D. | 该药物是由多种元素组成的混合物 |
 据报,2014年6月2日,瑞士帕耶讷,全球最大的太阳能飞机“阳光动力2号”首飞.据报道,这架飞机机翼上安装有1.7万块超薄且高效能的太阳能电池板,翼展长达72米.太阳能板在日间吸收能量,让飞机在晚间也可飞行,飞行时间不再受燃油量限制.请回答下列问题:
据报,2014年6月2日,瑞士帕耶讷,全球最大的太阳能飞机“阳光动力2号”首飞.据报道,这架飞机机翼上安装有1.7万块超薄且高效能的太阳能电池板,翼展长达72米.太阳能板在日间吸收能量,让飞机在晚间也可飞行,飞行时间不再受燃油量限制.请回答下列问题: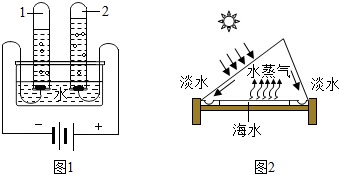 水是一种重要的资源.
水是一种重要的资源.