题目内容
13.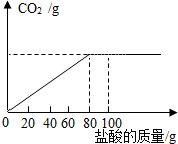 石灰石样品的主要成分是CaCO3.某化学课外兴趣小组将100g盐酸分成5等份,逐次加到用23克石灰石样品中(其他成分不与盐酸反应),得到部分数据与图象如下.请根据有关信息回答问题.
石灰石样品的主要成分是CaCO3.某化学课外兴趣小组将100g盐酸分成5等份,逐次加到用23克石灰石样品中(其他成分不与盐酸反应),得到部分数据与图象如下.请根据有关信息回答问题. | 第一次 | 第二次 | 第三次 | |
| 加入盐酸的质量(g) | 20 | 20 | 20 |
| 剩余固体的质量(g) | 18 | 13 | 8 |
(2)求该盐酸中溶质的质量分数(写出计算过程,计算结果保留一位小数).
分析 (1)由图象可知,加入80g盐酸时恰好反应,每20g盐酸反应掉5g碳酸钙,故加入80g盐酸时反应掉20g碳酸钙,剩余固体的质量为3g,即为杂质的质量;
(2)由杂质的质量可知碳酸钙的质量,根据化学方程式利用碳酸钙的质量计算出氯化氢的质量,进而求质量分数.
解答 解:(1)由图象可知,加入80g盐酸时恰好反应,每20g盐酸反应掉5g碳酸钙,故加入80g盐酸时反应掉20g碳酸钙,剩余固体的质量为3g,即为杂质的质量;
故答案为:3;
(2)碳酸钙的质量为:23g-3g=20g,
设40g盐酸中氯化氢的质量为x,
CaCO3+2HC1═CaCl2+CO2↑+H2O
100 73
20g x
$\frac{100}{20g}$=$\frac{73}{x}$
x=14.6g
所加盐酸的溶质质量分数为:$\frac{14.6g}{80g}$×100%=18.3%.
答:所加盐酸的溶质质量分数为18.3%.
点评 根据数据列表或关系图,找出反应中某物质的质量是这一类问题的解决方法.

练习册系列答案
相关题目
1.下列方程式合理的是( )
| A. | Ca(OH)2+Na2CO3═CaCO3↓+2NaOH | B. | 4Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 | ||
| C. | K2SO4+CuCl2═CuSO4+2KCl | D. | Cu+FeCl2═Fe+CuCl2 |
8.下列有关钢铁的叙述不正确的是( )
| A. | 生铁和钢都属于合金 | B. | 在钢管表面镀锌可以防止锈蚀 | ||
| C. | 铁锈的结构疏松多孔 | D. | 铁丝在氧气中燃烧生成氧化铁 |
18.某种气体在加压情况发生变化的微观示意图如图,下列分析中正确的是( )

| A. | 继续加压②后产生两种新分子 | |
| B. | 化学反应方程式可表示为2AB2$\frac{\underline{\;加压\;}}{\;}$A2B4 | |
| C. | 加压①后气体分子微粒的体积变小 | |
| D. | 加压①②后气体分子的间隔没有发生变化 |
2.下表是小明同学在除杂时所选用的试剂,其中正确的是( )
| 选项 | 物质 | 杂质 | 试剂 |
| A | K2SO4溶液 | (NH4)2SO4 | Ba(OH)2溶液 |
| B | CaO固体 | CaCO3 | 稀HCl |
| C | FeSO4溶液 | CuSO4 | Fe粉 |
| D | CO2气体 | HCl | NaOH溶液 |
| A. | A | B. | B | C. | C | D. | D、 |
3.除去下列物质中的少量杂质,所选用试剂及操作方法均正确的是( )
| 选项 | 物质(括号内为杂质) | 选用试剂 | 操作方法 |
| A | CO2(CO) | 过量O2 | 点燃 |
| B | CaO(CaCO3) | 足量蒸馏水 | 过滤、蒸发 |
| C | FeCl2溶液(CuCl2溶液) | 足量铁粉 | 过滤 |
| D | NaCl溶液(MgSO4溶液) | 适量BaCl2溶液 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
