题目内容
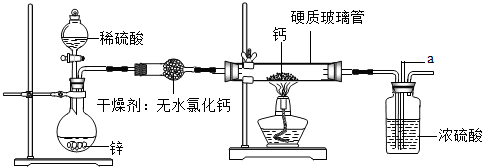
(2012?昌平区一模)氢化钙(CaH2)是一种储氢材料,是登山运动员常用的能源提供剂.甲、乙两位同学选用如下装置,用氢气与金属钙加热制备氢化钙.实验结束后,两位同学对硬质玻璃管中的固体进行如下探究:
[提出问题]硬质玻璃管中的Ca是否完全转化为CaH2?
[查阅资料]
①金属钙活动性很强,遇水反应生成氢氧化钙,同时产生一种气体;
②氢化钙要密封保存,遇水反应放出氢气.
[猜想与实验].
(1)固体为Ca和CaH2.
(2)固体为CaH2.
甲同学的探究活动如下:
甲同学的结论:猜想1正确,固体为Ca和CaH2.
[实验反思]
乙同学认为由以上探究活动还不能得出猜想1正确,理由是
[反思讨论]
(1)写出CaH2与水反应的化学方程式
(2)登山运动员常用氢化钙固体作能源提供剂,与氢气相比,其优点是
(3)制备CaH2装置中,玻璃管a的作用是

[提出问题]硬质玻璃管中的Ca是否完全转化为CaH2?
[查阅资料]
①金属钙活动性很强,遇水反应生成氢氧化钙,同时产生一种气体;
②氢化钙要密封保存,遇水反应放出氢气.
[猜想与实验].
(1)固体为Ca和CaH2.
(2)固体为CaH2.
甲同学的探究活动如下:
| 实验操作 | 实验现象 | 实验结论及解释 |
| ①取少量硬质玻璃管中的固体于试管中,滴入少量的水,收集产生的气体,并用燃着的木条点燃 | 气体燃烧,产生淡蓝色火焰 气体燃烧,产生淡蓝色火焰 |
有氢气生成 |
| ②继续向溶液中滴加酚酞 | 呈红色 | 生成 Ca(OH)2 Ca(OH)2 (填化学式) |
[实验反思]
乙同学认为由以上探究活动还不能得出猜想1正确,理由是
若固体为CaH2,遇水反应也会产生相同的现象
若固体为CaH2,遇水反应也会产生相同的现象
.请你帮助乙设计实验,写出主要的实验步骤、现象和相应的结论:取等质量的氢化钙和待测固体,分别放入两支试管中,加入足量的水,使其充分反应,收集产生的气体,比较反应产生气体的体积.若体积相等,说明玻璃管中Ca完全转化为CaH2;若不相等,则说明Ca未完全转化为CaH2
取等质量的氢化钙和待测固体,分别放入两支试管中,加入足量的水,使其充分反应,收集产生的气体,比较反应产生气体的体积.若体积相等,说明玻璃管中Ca完全转化为CaH2;若不相等,则说明Ca未完全转化为CaH2
.[反思讨论]
(1)写出CaH2与水反应的化学方程式
CaH2+2H2O═Ca(OH)2+2H2↑
CaH2+2H2O═Ca(OH)2+2H2↑
.(2)登山运动员常用氢化钙固体作能源提供剂,与氢气相比,其优点是
便于携带、避免爆炸危险
便于携带、避免爆炸危险
.(3)制备CaH2装置中,玻璃管a的作用是
检验装置的气密性
检验装置的气密性
.分析:[猜想与实验]:
根据氢气的可燃性和燃烧时的现象分析解答;
根据题目所给信息和反应前后元素种类不变、碱性物质可使酚酞变红分析解答;
[实验反思]
根据氢化钙与水反应的现象与钙与水反应的现象考虑结论是否正确;设计对比实验进行分析:取等质量的氢化钙和待测固体,加入足量的水,使其充分反应,若生成氢气的体积相等,说明固体为氢化钙;
[反思讨论]
(1)根据氢化钙与水反应的原理书写方程式;
(2)根据气体体积大不容易携带而固体体积小携带方便考虑;
(3)做实验时,装置的气密性要良好,装置气密性检验有多种方法,原理都是根据装置内外的压强差形成水柱或气泡,据此分析a的作用.
根据氢气的可燃性和燃烧时的现象分析解答;
根据题目所给信息和反应前后元素种类不变、碱性物质可使酚酞变红分析解答;
[实验反思]
根据氢化钙与水反应的现象与钙与水反应的现象考虑结论是否正确;设计对比实验进行分析:取等质量的氢化钙和待测固体,加入足量的水,使其充分反应,若生成氢气的体积相等,说明固体为氢化钙;
[反思讨论]
(1)根据氢化钙与水反应的原理书写方程式;
(2)根据气体体积大不容易携带而固体体积小携带方便考虑;
(3)做实验时,装置的气密性要良好,装置气密性检验有多种方法,原理都是根据装置内外的压强差形成水柱或气泡,据此分析a的作用.
解答:解:[猜想与实验]:
由实验结论可知,生成的气体是氢气,而氢气具有可燃性,且燃烧时火焰呈淡蓝色;
由题意可知:金属钙遇水反应生成氢氧化钙;氢化钙要密封保存,遇水反应放出氢气,依据反应前后元素种类不变可知:氢化钙与水反应生成氢氧化钙和氢气,而氢氧化钙溶液显碱性,碱性物质可使酚酞变红;
故答案为:
[实验反思]
由上述分析可知:氢化钙与水反应也能生成氢氧化钙和氢气,与钙和水水反应现象相同,所以以上探究活动还不能得出猜想1正确;可设计对比实验进行分析:取等质量的氢化钙和待测固体,加入足量的水,使其充分反应,若生成氢气的体积相等,说明玻璃管中Ca完全转化为CaH 2,固体为氢化钙;
故答案为:
若固体为CaH2,遇水反应也会产生相同的现象;
取等质量的氢化钙和待测固体,分别放入两支试管中,加入足量的水,使其充分反应,收集产生的气体,比较反应产生气体的体积.若体积相等,说明玻璃管中Ca完全转化为CaH 2;若不相等,则说明Ca未完全转化为CaH2;
[反思讨论]
(1)氢化钙与水反应生成氢氧化钙和氢气,方程式是CaH2+2H2O═Ca(OH)2+2H2↑;
(2)气体体积大不容易携带而固体体积小携带方便,且氢气具有可燃性,遇明火可能发生爆炸;
(3)检验装置的气密性时可这样操作:先在广口瓶中注入水浸没导管下端,双手捂住烧瓶,烧瓶内气体受热膨胀,使广口瓶瓶中气体压强增大,在a玻璃管中形成一段水柱,说明装置气密性良好;
故答案为:
(1)CaH2+2H2O═Ca(OH)2+2H2↑;
(2)便于携带、避免爆炸危险;
(3)检验装置的气密性.
由实验结论可知,生成的气体是氢气,而氢气具有可燃性,且燃烧时火焰呈淡蓝色;
由题意可知:金属钙遇水反应生成氢氧化钙;氢化钙要密封保存,遇水反应放出氢气,依据反应前后元素种类不变可知:氢化钙与水反应生成氢氧化钙和氢气,而氢氧化钙溶液显碱性,碱性物质可使酚酞变红;
故答案为:
| 实验现象 | 实验结论及解释 |
| 冒气泡;气体燃烧,产生淡蓝色火焰 | |
| Ca(OH)2 |
由上述分析可知:氢化钙与水反应也能生成氢氧化钙和氢气,与钙和水水反应现象相同,所以以上探究活动还不能得出猜想1正确;可设计对比实验进行分析:取等质量的氢化钙和待测固体,加入足量的水,使其充分反应,若生成氢气的体积相等,说明玻璃管中Ca完全转化为CaH 2,固体为氢化钙;
故答案为:
若固体为CaH2,遇水反应也会产生相同的现象;
取等质量的氢化钙和待测固体,分别放入两支试管中,加入足量的水,使其充分反应,收集产生的气体,比较反应产生气体的体积.若体积相等,说明玻璃管中Ca完全转化为CaH 2;若不相等,则说明Ca未完全转化为CaH2;
[反思讨论]
(1)氢化钙与水反应生成氢氧化钙和氢气,方程式是CaH2+2H2O═Ca(OH)2+2H2↑;
(2)气体体积大不容易携带而固体体积小携带方便,且氢气具有可燃性,遇明火可能发生爆炸;
(3)检验装置的气密性时可这样操作:先在广口瓶中注入水浸没导管下端,双手捂住烧瓶,烧瓶内气体受热膨胀,使广口瓶瓶中气体压强增大,在a玻璃管中形成一段水柱,说明装置气密性良好;
故答案为:
(1)CaH2+2H2O═Ca(OH)2+2H2↑;
(2)便于携带、避免爆炸危险;
(3)检验装置的气密性.
点评:解答时注意分析题目所给信息并结合所学知识,对信息加以整合,依据题意分析问题、解决问题.

练习册系列答案
 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案
相关题目