题目内容
小 黄同学为了测定某混合物(Na2CO3与NaOH混合)中碳酸钠的质量分数,进行了如下实验:称取了20g样品配成溶液,然后逐渐加入一定量质量分数为20.8%的BaCl2溶液(已知:Na2CO3+BaCl2=2NaCl+BaCO3↓),充分反应.在此过程中他进行了三次数据测定,结果如下表:
黄同学为了测定某混合物(Na2CO3与NaOH混合)中碳酸钠的质量分数,进行了如下实验:称取了20g样品配成溶液,然后逐渐加入一定量质量分数为20.8%的BaCl2溶液(已知:Na2CO3+BaCl2=2NaCl+BaCO3↓),充分反应.在此过程中他进行了三次数据测定,结果如下表:
| 测定次数 | 第1次 | 第2次 | 第3次 |
| 加入BaCl2溶液的质量/g | 60 | 120 | 150 |
| 生成沉淀的质量/g | 11.82 | 19.7 | 19.7 |
请分析数据,回答下列问题:
(1)第一次测定数据后所得溶液中含有溶质是NaOH, (填化学式);
(2)此实验中,实际参加反应的BaCl2溶液的质量为 ;
(3)样品中碳酸钠的质量分数为多少?(写出计算过程)
| 由图表数据可知:第1次加入60gBaCl2溶液生成沉淀11.82g,说明60gBaCl2溶液恰好生成碳酸钡沉淀11.82g,第2次加入19.7gBaCl2溶液,生成沉淀的质量应该是11.82g×2=23.64g,而实际反应生成了19.7g沉淀,说明混合物中Na2CO3已反应完,BaCl2溶液过量,说明碳酸钠最多生成19.7g碳酸钡,据碳酸钡的质量可计算出实际参加反应的BaCl2的质量,碳酸钠的质量,进而计算出BaCl2溶液的质量,碳酸钠的质量分数. | |
| 解答: | 解:(1)混合物中加入BaCl2溶液与碳酸钠发生反应生成碳酸钡沉淀,与氢氧化钠不反应;由图表数据可知:第1次加入60gBaCl2溶液生成沉淀11.82g,第2次BaCl2溶液的质量增加,沉淀的质量也增加,说明在第1次时BaCl2溶液不足,碳酸钠未完全反应,故反应后所得溶液中含有溶质NaOH,NaCl、Na2CO3; (2)第1次加入60gBaCl2溶液生成沉淀11.82g,说明60gBaCl2溶液恰好生成碳酸钡沉淀11.82g,第2次加入19.7gBaCl2溶液,生成沉淀的质量应该是11.82g×2=23.64g,而实际反应生成了19.7g沉淀,说明混合物中Na2CO3已反应完,BaCl2溶液过量,说明碳酸钠最多生成19.7g碳酸钡; 设实际参加反应的BaCl2溶液的质量为x,样品中碳酸钠的质量为y Na2CO3+BaCl2=2NaCl+BaCO3↓ 106 208 197 y x
实际参加反应的BaCl2溶液的质量为:20.8g÷20.8%=100g (3)样品中碳酸钠的质量分数是: 故答案为: (1)NaCl、Na2CO3; (2)100g; (3)样品中碳酸钠的质量分数是53%. |

 阅读快车系列答案
阅读快车系列答案小黄同学为了测定某混合物(Na2CO3与NaOH混合)中碳酸钠的质量分数,进行了如下实验:称取了20g样品配成溶液,然后逐渐加入一定量质量分数为20.8%的BaCl2溶液(已知:Na2CO3+BaCl2=2NaCl+BaCO3↓),充分反应.在此过程中他进行了三次数据测定,结果如下表:
|
测定次数 |
第1次 |
第2次 |
第3次 |
|
加入BaCl2溶液的质量/g |
60 |
120 |
150 |
|
生成沉淀的质量/g |
11.82 |
19.7 |
19.7 |
请分析数据,回答下列问题:
(1)第一次测定数据后所得溶液中含有溶质是NaOH, (填化学式);
(2)此实验中,实际参加反应的BaCl2溶液的质量为 ;
(3)样品中碳酸钠的质量分数为多少?(写出计算过程)
小黄同学为了测定某混合物(Na2CO3与NaOH混合)中碳酸钠的质量分数,进行了如下实验:称取了20g样品配成溶液,然后逐渐加入一定量质量分数为20.8%的BaCl2溶液(已知:Na2CO3+BaCl2=2NaCl+BaCO3↓),充分反应.在此过程中他进行了三次数据测定,结果如下表:
| 测定次数 | 第1次 | 第2次 | 第3次 |
| 加入BaCl2溶液的质量/g | 60 | 120 | 150 |
| 生成沉淀的质量/g | 11.82 | 19.7 | 19.7 |
(1)第一次测定数据后所得溶液中含有溶质是NaOH,______(填化学式);
(2)此实验中,实际参加反应的BaCl2溶液的质量为______;
(3)样品中碳酸钠的质量分数为多少?(写出计算过程)
| 测定次数 | 第1次 | 第2次 | 第3次 |
| 加入BaCl2溶液的质量/g | 60 | 120 | 150 |
| 生成沉淀的质量/g | 11.82 | 19.7 | 19.7 |
(1)第一次测定数据后所得溶液中含有溶质是NaOH,______(填化学式);
(2)此实验中,实际参加反应的BaCl2溶液的质量为______;
(3)样品中碳酸钠的质量分数为多少?(写出计算过程)
 19.7g
19.7g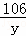 =
=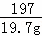 y=10.6g
y=10.6g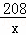 =
=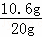 ×100%=53%
×100%=53%