题目内容
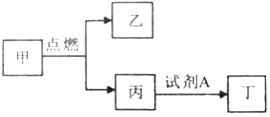
【题目】工业上利用电石(CaC2)制备高纯碳酸钙的流程如下:

已知:①![]()
②![]()
(1)乙炔(C2H2)是一种常见的燃料,写出乙炔完全燃烧的化学方程式_____;
(2)流程中可循环使用的物质是_____(填化学式);
(3)若将电石长期露置于空气中,会发生一系列变化,最终所得固体中一定含有的物质是_____;
(4)电石应该_____保存。
【答案】 NH4Cl CaCO3 密封
NH4Cl CaCO3 密封
【解析】
(1)乙炔(C2H2)是一种常见的燃料,乙炔在氧气中完全燃烧生成二氧化碳和水,化学方程式: ;
;
(2)残渣中加入氯化铵生成氨气和氯化钙,氯化钙、水、二氧化碳、氨气反应产生碳酸钙和氯化铵,流程中可循环使用的物质是氯化铵:NH4Cl;
(3)若将电石长期露置于空气中,会与空气中的水蒸气反应,产生乙炔和氢氧化钙,氢氧化钙与空气中的二氧化碳反应产生碳酸钙,最终所得固体中一定含有的物质是碳酸钙:CaCO3;
(4)电石能与空气中的水蒸气反应,应该密封保存。

练习册系列答案
 每课必练系列答案
每课必练系列答案
相关题目