题目内容
12.在硫酸铁【Fe2(SO4)3】和硫酸亚铁【FeSO4】的混合物中:(1)若铁元素的质量分数为a%,则硫元素的质量分数为$\frac{1-a%}{3}$.
(2)若氧元素的质量分数为b%,则铁元素的质量分数为1-1.5b%.
分析 根据FeSO4和Fe2(SO4)3两物质的组成特点,可知混合物中含有铁、硫、氧三种元素,硫元素与氧元素的质量比为1:2,铁元素的质量分数为a%,则硫元素与氧元素的质量分数为1-a%;可求硫元素的质量分数为.
(2)混合物中氧元素的质量分数为b%,可计算出混合物中硫元素质量分数0.5b%,进而可计算出该混合物中铁元素的质量分数.
解答 解:(1)在FeSO4和Fe2(SO4)3组成的混合物中,可知混合物中含有铁、硫、氧三种元素,硫元素与氧元素的质量比=32:(16×4)=1:2,铁元素的质量分数为a%,则硫元素与氧元素的质量分数为1-a%;硫元素的质量分数为$\frac{1-a%}{3}$.
(2)在FeSO4和Fe2(SO4)3组成的混合物中,硫元素与氧元素的质量比=32:(16×4)=1:2,混合物中氧元素的质量分数为b%,可计算出混合物中硫元素质量分数0.5b%,该混合物中铁元素的质量分数为1-b%-0.5b%=1-1.5b%.
故填:$\frac{1-a%}{3}$;1-1.5b%.
点评 根据混合物组成中两化合物的中组成元素的特别关系,确定混合物中元素的质量分数,此类问题通过存在这种特点.

练习册系列答案
相关题目
3.下列实验仅利用家庭生活用品不可能完成的是( )
| A. | 用肥皂水鉴别自来水是软水还是硬水 | |
| B. | 探究蜡烛火焰各层温度的高低 | |
| C. | 用食腊除去热水瓶中的水垢 | |
| D. | 用加热法修补破裂的电木插座 |
20.X元素的原子最外层有6个电子,Y元素的原子最外层有三个电子,则由X和Y两种元素组成的化合物的化学式可能为( )
| A. | XY2 | B. | X2Y3 | C. | Y2X | D. | Y2X3 |
17.物质的用途与性质密切相关.下列说法不正确是( )
| A. | 铁制品表面涂“银粉”(铝粉)防生锈,是由于铝的化学性质比铁稳定 | |
| B. | 二氧化碳用于灭火,是由于二氧化碳不可燃、不助燃且密度比空气大 | |
| C. | 氮气常用作保护气,是由于氮气的化学性质不活泼 | |
| D. | 铜用于制导线,是由于铜有良好的导电性 |
4.下列说法正确的是( )
| A. | 氯化钠溶液会加快钢铁的锈蚀 | |
| B. | 生铁能完全溶解在足量的稀硫酸中 | |
| C. | 高炉炼铁中所需的高温和CO的生成都与焦炭有关 | |
| D. | 多数合金的硬度低于组成它们的成分金属的硬度 |
20.实验室制氧气主要操作如下:①给试管加热 ②连接仪器检查装置气密性 ③装配好仪器 ④装药品 ⑤收集氧气 ⑥熄灭酒精灯 ⑦将导管移出水面.正确顺序为( )
| A. | ②④③①⑤⑥⑦ | B. | ④②③①⑤⑥⑦ | C. | ②④③①⑤⑦⑥ | D. | ④③②①⑤⑦⑥ |
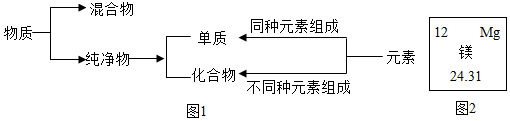
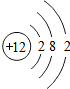 ,其氯化物的化学式为MgCl2.
,其氯化物的化学式为MgCl2.