题目内容
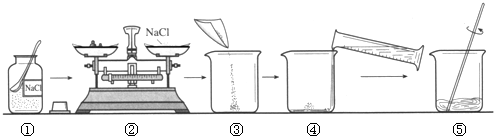
如图是配制50g溶质质量分数为15%的氯化钠溶掖的操作过程示意图.
试回答:
(1)B操作中应称量NaCl的质量是
(2)D操作中应选用
(3)E操作中玻璃棒的作用是

试回答:
(1)B操作中应称量NaCl的质量是
7.5
7.5
g,称量时若指针偏右,应进行的操作是增加氯化钠的质量
增加氯化钠的质量
(2)D操作中应选用
50mL
50mL
(10mL、50mL、100mL)量筒量取实验所需的水.(3)E操作中玻璃棒的作用是
搅拌、加快溶解速度
搅拌、加快溶解速度
.分析:根据已有的知识进行分析,溶质的质量=溶质质量分数×溶液的质量,并据天平的使用分析解答;选择量筒时,量筒的量程要大于所取液体的体积,读数时视线要跟凹液面的最低处保持水平,为加快溶解速度,应用玻璃棒搅拌.
解答:解:(1)B操作为称取固体氯化钠的质量,根据公式可计算需要氯化钠的质量为50g×15%=7.5g,称量时氯化钠放在左盘,指针偏向分度盘的右边说明氯化钠不足,应增加药品的量;
(2)经计算所需水的体积为42.5mL,所以应该选择50mL量筒来量取;
(3)玻璃棒搅拌的作用是搅拌、加快溶解速度;
故答案为:(1)7.5,增加氯化钠的质量;
(2)50mL.
(3)搅拌、加快溶解速度.
(2)经计算所需水的体积为42.5mL,所以应该选择50mL量筒来量取;
(3)玻璃棒搅拌的作用是搅拌、加快溶解速度;
故答案为:(1)7.5,增加氯化钠的质量;
(2)50mL.
(3)搅拌、加快溶解速度.
点评:本题考查了溶液的配制,完成此题,可以依据已有的知识结合溶质质量分数公式及仪器的使用进行解答.

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目