题目内容
利用氯化钠制备碳酸钠的同时可以得到氯化铵,如表为氯化铵的溶解度:
(1)向100g水中不断加入氯化铵固体或改变温度,得到如图相应的溶液A~E.溶液C是 (填“饱和”或“不饱和”)溶液.
(2)溶液E中析出晶体 g,将此时盛有溶液E的小烧杯放入盛有水的大烧杯中,向大烧杯内加入NaOH固体,小烧杯内的固体溶解,原因是 .

| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 溶解度/g | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 | 60.2 | 65.6 |
(2)溶液E中析出晶体
考点:饱和溶液和不饱和溶液,溶解时的吸热或放热现象,晶体和结晶的概念与现象
专题:溶液、浊液与溶解度
分析:根据已有的知识进行分析,根据溶解度确定溶液是否是饱和溶液;、析出晶体的质量,氢氧化钠固体溶于水会放出大量的热,据此解答.
解答:解:(1)60℃时氯化铵的溶解度是55.2g,经过操作得到的100g水中含有的氯化铵的质量为40g+5g=45g,故形成的是不饱和溶液,故填:不饱和;
(2)得到的溶液D中含有氯化铵固体的质量是55g,40℃时氯化铵的溶解度是45.8g,故析出晶体的质量是55g-45.8g=9.2g;氢氧化钠固体溶于水会放出大量的热,而氯化铵的溶解度随温度的升高而增大,固体会继续溶解,故填:9.2;氢氧化钠溶于水放热,氯化铵的溶解度随温度的升高而增大.
(2)得到的溶液D中含有氯化铵固体的质量是55g,40℃时氯化铵的溶解度是45.8g,故析出晶体的质量是55g-45.8g=9.2g;氢氧化钠固体溶于水会放出大量的热,而氯化铵的溶解度随温度的升高而增大,固体会继续溶解,故填:9.2;氢氧化钠溶于水放热,氯化铵的溶解度随温度的升高而增大.
点评:本题考查了饱和溶液与溶解度的关系,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目

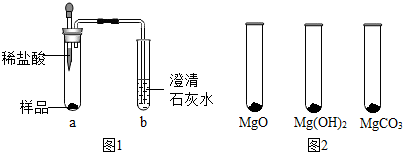 体操运动员在完成单杠、吊环项目时常用“镁粉”搓手,以起到防滑效果.某种“镁粉”中可能含有Mg、MgO、Mg(OH)2、MgCO3中的一种或两种固体,实验小组对其成分展开了探究.
体操运动员在完成单杠、吊环项目时常用“镁粉”搓手,以起到防滑效果.某种“镁粉”中可能含有Mg、MgO、Mg(OH)2、MgCO3中的一种或两种固体,实验小组对其成分展开了探究. 如图是甲、乙、丙三种固体物质的溶解度曲线,请回答:
如图是甲、乙、丙三种固体物质的溶解度曲线,请回答: