题目内容
要使Fe3O4和Fe2O3中所含铁元素质量相等,则Fe3O4与Fe2O3质量比为( )
分析:利用一定质量的化合物中元素的质量为化合物的质量与化合物中质量分数的乘积,根据两物质的化学式,可通过两物质中铁元素质量相等建立等式,计算出两物质的质量比.
解答:解:假设Fe3O4与Fe2O3的质量分别为x、y,则
x×
×100%=y×
×100%
x:y=29:30.
故选C.
或者
根据Fe3O4和Fe2O3中铁元素质量相等,所以对应铁原子也相等,即Fe3O4和Fe2O3的分子个数比为2:3,也就是两者存在2Fe3O4和3Fe2O3的比例关系.则两物质的质量比为
=
=
即选C
x×
| 56×3 |
| 232 |
| 56×2 |
| 160 |
x:y=29:30.
故选C.
或者
根据Fe3O4和Fe2O3中铁元素质量相等,所以对应铁原子也相等,即Fe3O4和Fe2O3的分子个数比为2:3,也就是两者存在2Fe3O4和3Fe2O3的比例关系.则两物质的质量比为
| (56×3+16×4)×2 |
| (56×2+16×3)×3 |
| 232×2 |
| 160×3 |
| 29 |
| 30 |
即选C
点评:利用化合物中组成元素的质量分数,可由一定质量的化合物计算该化合物中所含元素的质量;利用两物质中共同元素的质量关系,可计算两化合物的质量关系.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
要使Fe3O4和Fe 2O3中所含铁元素质量相等,则Fe3O4与Fe 2O3质量比为( )
| A.2∶3 | B.4∶5 | C.29∶30 | D.3∶2 |
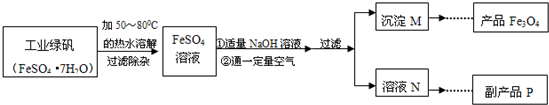
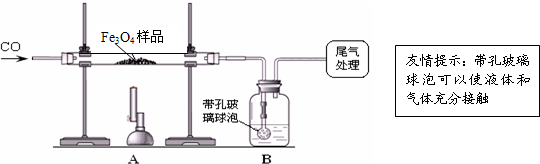
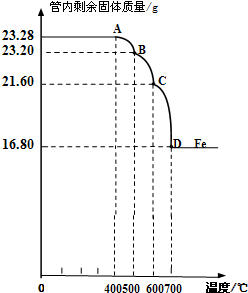 质量差会偏小而影响计算、分析,你认为他们的理由是
质量差会偏小而影响计算、分析,你认为他们的理由是