题目内容
18.钢铁工业在国民经济中占有重要地位.(1)工业上用一氧化碳和赤铁矿炼铁反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(2)3.75g某钢样在纯氧中燃烧,得到0.044g二氧化碳.求此钢样中碳的质量分数.(写出计算过程,计算结果保留二位小数)
分析 (1)工业上用一氧化铁和赤铁矿炼铁是一氧化碳和氧化铁在高温下生成铁和二氧化碳;
(2)根据二氧化碳求算碳的质量,进而求算出样品中碳的质量分数.碳的质量两种求算方式,一是化学式计算,二是化学方程式计算.
解答 解:
(1)一氧化铁和赤铁矿炼铁是一氧化碳和氧化铁在高温下生成铁和二氧化碳,对应的化学方程式为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(2)方法一:用化学式计算
0.44g二氧化碳中所含的碳元素的质量为0.044g×$\frac{12}{12+16×2}$×100%=0.012g
方法二:化学方程式计算
设碳的质量为x
C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2
12 44
x 0.044g
$\frac{12}{44}$=$\frac{x}{0.044g}$
x=0.012g
则此钢样中碳的质量分数为$\frac{0.012g}{3.75g}$×100%=0.32%
答:此钢样中碳的质量分数为0.32%.
答:(1)工业上用一氧化碳和赤铁矿炼铁反应的化学方程式为 Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(2)3.75g某钢样在纯氧中燃烧,得到0.044g二氧化碳.求此钢样中碳的质量分数为0.32%.
点评 题目2的解题方法不要受化学方程式计算干扰,解题没有固定的模式,灵活处理即可.

练习册系列答案
 走进文言文系列答案
走进文言文系列答案
相关题目
8.“分类”是化学学习和研究的重要方法之一,下列分类中正确的是( )
| A. | 硫酸铜、食盐、纯碱-盐 | B. | 硫酸铵、硝酸钾、尿素-氮肥 | ||
| C. | 空气、消石灰、碘酒-混合物 | D. | 氨气、小苏打、苛性钠-碱 |
6.如图装置在实验室中经常用到,对该装置的说法错误的是( )
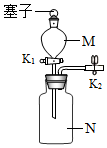

| A. | K2关闭、K1打开、塞子塞紧时,若M中的水不能流下则装置气密性好 | |
| B. | 若M中盛放双氧水,N中盛放二氧化锰,则可以制取氧气 | |
| C. | 若M中盛放稀盐酸,N中盛放块状大理石,则可以制取二氧化碳 | |
| D. | N中储满不溶于水的气体时,将水不断由M注入N中,即可将气体排出 |
3.2015年中国科学家屠呦呦因青蒿索(C15H22O5)和双氢青蒿素(C15H24O5)而荣获了诺贝尔奖.下列有关说法中不正确的是( )
| A. | 青蒿素比双氢青蒿素少两个氢原子 | |
| B. | 青蒿素和双氢青蒿素都是由碳、氢、氧三种元素组成的 | |
| C. | 青蒿素和双氢青蒿素中碳、氧原子个数比都为3:1 | |
| D. | 青蒿素中氧元素的质量分数比双氢青蒿素中氧元素的质量分数大 |
10.香料化学家已经开发出多种人工香料,如丁酸甲酯(化学式为C5H10O2)具有苹果香味.下列有关丁酸甲酯的说法正确的是( )
| A. | 丁酸甲酯属于氧化物 | |
| B. | 丁酸甲酯由17个原子构成 | |
| C. | 丁酸甲酯中氧元素的质量分数约为58.82% | |
| D. | 丁酸甲酯中碳元素、氢元素和氧元素的质量比为30:5:16 |
14.某物质经分析只含有一种元素,则它( )
| A. | 一定是纯净物 | B. | 一定是混合物 | C. | 不可能是化合物 | D. | 可能是纯净物 |
 水是重要的自然资源.
水是重要的自然资源.