题目内容
在一密闭容器中,盛放A、B、C三种物质,在一定条件下充分反应后,各物质质量变化如表,则关于此反应,下列说法正确的是( )
| 物质 | A | B | C | 新物质D |
| 反应前物质的质量(g) | 30 | 30 | 31 | 0 |
| 反应后物质的质量(g) | 待测 | 33 | 1 | 22 |
| A、反应后待测的A质量为35g |
| B、B物质一定为单质 |
| C、反应中物质B、C的质量之比为33:1 |
| D、若B与D的相对分子质量之比为1﹕22,则反应中B与D化学计量数之比为3﹕2 |
考点:质量守恒定律及其应用
专题:化学用语和质量守恒定律
分析:由于开始ABC都是30g,随着反应的进行,BD质量都是增加的,而C是质量减少的,所以可以根据质量守恒推算A的待测数据.同时质量减少的为反应物,而质量增加的都是生成物,从而进一步推断反应的类型以及部分物质的种类.
解答:解:由于C的质量减少了30g,而B只增加了3g,D增加了22g,所以A必须增加5g.ABD都增加,而只有C减少,说明ABD是生成物,C是反应物.
A、A本来是30g,又生成了5g所以待测数值为35g,正确;
B、由于C是反应物,而A、B、D都是生成物,所以是一变多,为分解反应,则B物质可能为单质.故错误;
C、反应中物质B、C的质量之比为(33-30)g:(31-1)g=1:10.故错误;
D、若B与D的相对分子质量之比为1﹕22,而B与D的质量之比为3:22,设反应的化学方程式为xC═yA+zB+wD.则xC═yA+zB+wD
z 22w
则
=
,解得
=
,则反应中B与D化学计量数之比为3﹕1,故错误.
故选:A.
A、A本来是30g,又生成了5g所以待测数值为35g,正确;
B、由于C是反应物,而A、B、D都是生成物,所以是一变多,为分解反应,则B物质可能为单质.故错误;
C、反应中物质B、C的质量之比为(33-30)g:(31-1)g=1:10.故错误;
D、若B与D的相对分子质量之比为1﹕22,而B与D的质量之比为3:22,设反应的化学方程式为xC═yA+zB+wD.则xC═yA+zB+wD
z 22w
则
| z |
| 22w |
| 3 |
| 22 |
| z |
| w |
| 3 |
| 1 |
故选:A.
点评:从题目的数据中分析物质的反应物还是生成物的类别,进而分析反应的质量关系和物质本身的类别.

练习册系列答案
 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案
相关题目
下列有关溶液的说法正确的是( )
| A、溶液都是均一、稳定的混合物 |
| B、饱和溶液就是不能再溶解任何物质的溶液 |
| C、同种物质的饱和溶液一定比不饱和溶液浓 |
| D、无色透明的液体都是溶液 |
在一定温度下,从500克M物质的饱和溶液中取出100克,剩下的溶液比原溶液( )
| A、溶质质量分数减小 |
| B、M的溶解度减小 |
| C、溶质质量减小 |
| D、溶液密度增大 |
下列叙述中,正确的是( )
| A、饱和溶液一定是浓溶液 |
| B、不饱和溶液一定是稀溶液 |
| C、氧化物都含有氧元素 |
| D、含有氧元素的化合物都是氧化物 |
将10克溶质质量分数为36%的浓盐酸稀释成15%的稀盐酸,需加水的质量为( )
| A、11克 | B、13克 |
| C、14克 | D、16 克 |
反应A+2B=C+2D中,若29克A与49克B全反应生成60克C,已知D的式量为18,则A的式量是( )
| A、29 | B、49 | C、58 | D、85 |
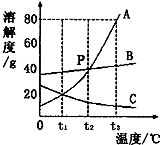 如图是 A、B、C三种物质的溶解度曲线,回答下列问题:
如图是 A、B、C三种物质的溶解度曲线,回答下列问题: ”和“
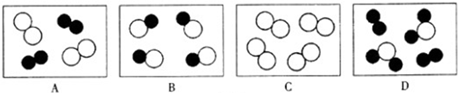
”和“ ”表示不同元素的原子,其中表示化合物的是
”表示不同元素的原子,其中表示化合物的是