题目内容
11.往AgNO3和Cu(NO3)2的混合溶液中加入一定量的锌粒,充分反应后过滤,往滤渣中加入稀盐酸,无气泡产生.你能得出的结论是( )| A. | 滤渣中一定有Zn | B. | 滤渣中一定有Ag和Cu | ||
| C. | 滤渣中可能有Cu | D. | 滤液中一定有Ag+和Cu2+ |
分析 在金属活动性顺序中,Zn>H>Cu>Ag,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来.
解答 解:金属活动性顺序中,Zn>H>Cu>Ag,往AgNO3和Cu(NO3)2的混合溶液中加入一定量的锌粒,锌先与硝酸银反应,当硝酸银反应完全后锌再与硝酸铜反应.充分反应后过滤,往滤渣中加入稀盐酸,无气泡产生,说明了锌没有剩余.
A、由上述分析可知,滤渣中一定没有Zn,故A错误;
B、由于锌没有剩余,所以滤渣中一定有Ag,可能有Cu,故B错误;
C、由上述分析可知,滤渣中可能有Cu,故C正确;
D、由于锌的量不能确定,滤液中可能有Ag+和Cu2+,故D错误.
故选:C.
点评 本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序的意义进行.

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目
1.厨房有一包无标识的白色粉末,经初步认定可能是氯化钠、碳酸钠、碳酸氢钠中的一种,小明对白色粉末的成分进行了探究.
【查阅资料】
1、碳酸钠、碳酸氢钠都能溶于水,且水溶液都呈碱性.
2、碳酸钙难溶于水,碳酸氢钠微溶于水.
3、碳酸氢钠与氢氧化钙的反应原理:
氢氧化钙少量时:2NaHCO3+Ca(OH)2═Na2CO3+CaCO3↓+2H2O
氢氧化钙过量时:NaHCO3+Ca(OH)2═NaOH+CaCO3↓+H2O
【实验探究】小明取适量白色粉末,配制成溶液,按表中所示实验方案进行探究.
(1)请完成表中空格.
(2)实验步骤2中可能发生反应的化学方程式为Na2CO3+2HCl=2NaCl+H2O+CO2↑,NaHCO3+HCl=NaCl+H2O+CO2↑(写出一个即可).实验步骤3中白色沉淀的成分是碳酸钙(填名称).
【实验反思】小明实验后发现上述实验方案并不能确定白色粉末的组成.经老师指导后,小明再取少量配制的溶液滴加氯化钙溶液,没有观察到明显现象,则该白色粉末是NaHCO3(或碳酸氢钠).
【查阅资料】
1、碳酸钠、碳酸氢钠都能溶于水,且水溶液都呈碱性.
2、碳酸钙难溶于水,碳酸氢钠微溶于水.
3、碳酸氢钠与氢氧化钙的反应原理:
氢氧化钙少量时:2NaHCO3+Ca(OH)2═Na2CO3+CaCO3↓+2H2O
氢氧化钙过量时:NaHCO3+Ca(OH)2═NaOH+CaCO3↓+H2O
【实验探究】小明取适量白色粉末,配制成溶液,按表中所示实验方案进行探究.
| 实验步骤 | 实验内容 | 实验现象 | 实验结论 |
| 1 | 取少量溶液,滴加无色酚酞溶液 | 溶液变红色 | 白色粉末肯定不是NaCl |
| 2 | 取少量溶液,滴加稀盐酸 | 有气泡产生 | / |
| 3 | 取少量溶液,滴加澄清石灰水 | 产生白色沉淀 | / |
(2)实验步骤2中可能发生反应的化学方程式为Na2CO3+2HCl=2NaCl+H2O+CO2↑,NaHCO3+HCl=NaCl+H2O+CO2↑(写出一个即可).实验步骤3中白色沉淀的成分是碳酸钙(填名称).
【实验反思】小明实验后发现上述实验方案并不能确定白色粉末的组成.经老师指导后,小明再取少量配制的溶液滴加氯化钙溶液,没有观察到明显现象,则该白色粉末是NaHCO3(或碳酸氢钠).
2.自来水消毒过程中发生反应的微观示意图如下,下列有关说法正确的是( )


| A. | 该反应说明原子在化学反应中可再分 | |
| B. | 反应物的分子个数比为3:2 | |
| C. | 此反应为置换反应 | |
| D. | 丁物质中氯元素的化合价+1 |
6.下列实验现象的描述正确的是( )
| A. | 铁丝在氧气中燃烧发出耀眼的白光 | |
| B. | 红磷在空气中燃烧产生大量白烟 | |
| C. | 生锈的铁钉投入稀盐酸中,溶液呈黄色,生成氯化亚铁 | |
| D. | 硫在空气中燃烧发出微弱的淡蓝色火焰,生成二氧化硫气体 |
16.在一个密闭的容器中放入A.B.C.D四种物质,在一定条件下发生化学反应,一段时间后,测得四种物质的质量如表
关于这个反应的说法正确的是( )
| 物质 | A | B | C | D |
| 反应前的质量/g | 20 | 2 | 3 | 36 |
| 反应后的质量/g | 待测 | 20 | 3 | 10 |
| A. | 物质C一定是反应中的催化剂 | B. | 物质B参加反应的质量是20g | ||
| C. | 这是一个分解反应 | D. | 物质A的待测的质量是16g |
3.除去括号内杂质选用的试剂正确的是( )
| A. | CaO(CaCO3)用稀盐酸 | B. | KCl(MgCl2)用氢氧化钠 | ||
| C. | Cu(NO3)2(AgNO3) 用铜粉 | D. | CO2(CO)用澄清石灰水 |
14.如图所示的粒子结构示意图中,属于原子的是( )
| A. | 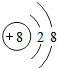 | B. | 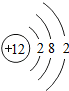 | C. |  | D. | 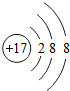 |
