题目内容
纯净的碳酸钙可用作牙膏中的磨牙剂.煅烧石灰石的某工艺流程如下(杂质与水不反应):

①操作a的名称为 .
②高温煅烧石灰石的化学方程式为 .煅烧完全后,取固体B于试管中,加入一定量水后,再滴加无色酚酞,看到的现象是 .
③你认为该工艺流程的目的是 .

①操作a的名称为
②高温煅烧石灰石的化学方程式为
③你认为该工艺流程的目的是
考点:物质的相互转化和制备,过滤的原理、方法及其应用,碳酸钙、生石灰、熟石灰之间的转化,书写化学方程式、文字表达式、电离方程式
专题:物质的制备
分析:①根据过滤可以将溶液和固体分离进行分析;
②根据碳酸钙在高温的条件下生成氧化钙和二氧化碳,氧化钙和水会生成氢氧化钙,氢氧化钙显碱性进行分析;
③根据该流程可以将碳酸钙的纯度提高进行分析.
②根据碳酸钙在高温的条件下生成氧化钙和二氧化碳,氧化钙和水会生成氢氧化钙,氢氧化钙显碱性进行分析;
③根据该流程可以将碳酸钙的纯度提高进行分析.
解答:解:①过滤可以将溶液和固体分离,经过操作a后得到了固体和液体,所以操作a的名称为:过滤;
②碳酸钙在高温的条件下生成氧化钙和二氧化碳,化学方程式为:CaCO3
CaO+CO2↑,氧化钙和水会生成氢氧化钙,氢氧化钙显碱性,能使无色酚酞变红色;
③该流程可以将碳酸钙的纯度提高,所以该工艺流程的目的是:获得高纯度碳酸钙.
故答案为:①过滤;
②CaCO3
CaO+CO2↑,溶液呈红色;
③获得高纯度碳酸钙.
②碳酸钙在高温的条件下生成氧化钙和二氧化碳,化学方程式为:CaCO3
| ||
③该流程可以将碳酸钙的纯度提高,所以该工艺流程的目的是:获得高纯度碳酸钙.
故答案为:①过滤;
②CaCO3
| ||
③获得高纯度碳酸钙.
点评:本题主要考查学生对分解反应类型的掌握,了解分解反应的特点,能正确书写方程式.同时体现了“绿色化学”的理念,培养学生的环保意识和节约意识.

练习册系列答案
相关题目
下列应用的原理(用符号表达式表示)及基本反应类型均正确的是( )
| A、碳酸钙与盐酸反应CaCO3+HCl→CaCl2+H2O+CO2↑ 分解反应 | |||
B、拉瓦锡测定空气中氧气含量实验Hg+O2
| |||
C、加热混有二氧化锰的氯酸钾制取氧气KClO3
| |||
D、氢气在氯气中燃烧H2+Cl2
|
某化学反应中,各物质质量随时间变化的曲线如图所示.其中说法一定正确的是( )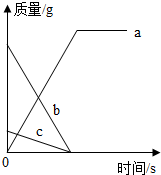

| A、该反应是分解反应 |
| B、物质c发生还原反应 |
| C、物质a的摩尔质量等于b和c的摩尔质量之和 |
| D、物质a中元素种类等于b和c中元素种类之和 |
关于物质的量描述正确的是( )
| A、物质的量常用符号N表示 |
| B、18 g H2O中含有1mol氢分子 |
| C、1 mol SO2中约含有6.02×1023个氧原子 |
| D、1mol任何物质都约含6.02×1023个微粒 |
关于二氧化碳说法正确的是( )
| A、实验室制法:木炭燃烧 |
| B、固态二氧化碳的俗名:干冰 |
| C、对环境影响:形成酸雨 |
| D、溶解度:随温度升高而变大 |
下列金属中,能被磁铁吸引的金属是( )
| A、铁片 | B、铝片 | C、铜片 | D、锌 |

 如图化学反应的溶液颜色变化体现了“魔法世界,魅力化学”.
如图化学反应的溶液颜色变化体现了“魔法世界,魅力化学”.