题目内容
11.工业制漂白粉的化学方程式为:2Ca(OH)2+2Cl2═X+CaCl2+2H2O,则X为( )| A. | CaClO | B. | Ca(ClO)2 | C. | Ca(ClO)3 | D. | Ca(ClO)4 |
分析 由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断生成物X的化学式.
解答 解:根据质量守恒定律反应前后原子个数不变和2Ca(OH)2+2Cl2═X+CaCl2+2H2O可知,每个X中含有1个钙原子和2个氯原子和2个氧原子,X是氯化钙,化学式是Ca(ClO)2.
故选:B
点评 只要是化学变化,就遵循质量守恒定律,根据化学方程式中反应物和生成物的化学式,可以判断出某种物质的种类.

练习册系列答案
相关题目
6.下列物质属于纯净物的是( )
| A. | 铁矿石 | B. | 自来水 | C. | 蒸馏水 | D. | 不锈钢 |
16.下列有关物质的用途与性质的说法正确的是( )
| A. | 因为“洗洁精”能溶解油污,所以“洗洁精”可用来洗涤餐具上的油污 | |
| B. | 二氧化碳能用于制碳酸饮料,说明二氧化碳显酸性 | |
| C. | 氧气能供给水中生物呼吸,说明氧气极易溶于水 | |
| D. | 金刚石可用于切割玻璃,说明金刚石硬度大 |
3.下列电池中,不属于由化学能转变为电能的是( )
| A. | 干电池 | B. | 蓄电池 | C. | 燃料电池 | D. | 太阳能电池 |
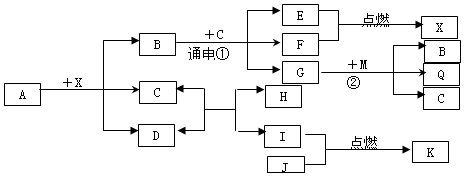
 A、B、C是初中化学学习中常见的三种氧化物,其中A是一种黑色粉末,B是一种导致温室效应的气体,C是一种液体.如图,三种物质与适当的物质在适当的条件下有如图所示的转化关系(其它反应物和反应条件略去).
A、B、C是初中化学学习中常见的三种氧化物,其中A是一种黑色粉末,B是一种导致温室效应的气体,C是一种液体.如图,三种物质与适当的物质在适当的条件下有如图所示的转化关系(其它反应物和反应条件略去). 干电池在生活中有多方面的应用,如图显示的是干电池的内部构造,请回答下列问题:
干电池在生活中有多方面的应用,如图显示的是干电池的内部构造,请回答下列问题: