题目内容
 氨气是一种有刺激性气味的无色气体,密度比空气小,它极易溶于水,形成的溶液叫氨水,实验室中常用加热氯化铵(NH4Cl)和氢氧化钙[Ca(OH)2]固体混合物的方法制取氨气.
氨气是一种有刺激性气味的无色气体,密度比空气小,它极易溶于水,形成的溶液叫氨水,实验室中常用加热氯化铵(NH4Cl)和氢氧化钙[Ca(OH)2]固体混合物的方法制取氨气.(1)实验室中制取氨气的发生装置可选用同
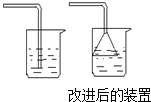
(2)小明想用实验来探究氨水在水中的溶解性,于是他直接将正在排出氨气的导管插入水中,结果造成试管
炸裂,其原因是
(3)该反应同时可生成一种氯化物和相对分子质量最小的氧化物,试写出该反应的化学方程式
考点:常用气体的发生装置和收集装置与选取方法,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)氨气是一种密度比空气小,极易溶于水的气体,所以只能用向下排气法收集;实验室用加热氯化氨和消石灰的固体混合物制取氨气,所以用高锰酸钾制氧装置制取;
(2)根据氨气极易溶于,会发生倒吸解答;在出气管连接漏斗可增大氨气与水的接触面积,防止逸散到空气中,吸收的更彻底;
(3)根据实验室里通常用加热氯化铵固体和氢氧化钙固体混合物的方法制取氨气,生成一种氯化物和相对分子质量最小的氧化物,写出该反应的化学方程式解答.
(2)根据氨气极易溶于,会发生倒吸解答;在出气管连接漏斗可增大氨气与水的接触面积,防止逸散到空气中,吸收的更彻底;
(3)根据实验室里通常用加热氯化铵固体和氢氧化钙固体混合物的方法制取氨气,生成一种氯化物和相对分子质量最小的氧化物,写出该反应的化学方程式解答.
解答:解:
(1)制取氨气用的药品是氯化氨和消石灰固体,反应条件是加热,故发生装置应选高锰酸钾制氧气的装置;氨气密度比空气小,易溶于水,所以只能用向下排空气法收集;
(2)氨气极易溶于水,水会到吸入试管,将试管炸裂;为了防止其逸散到空气中污染空气,可以用水吸收,在出气管连接漏斗可增大氨气与水的接触面积,防止逸散到空气中,吸收的更彻底;
(3)实验室里通常用加热氯化铵固体和氢氧化钙固体混合物的方法制取氨气.其化学方程式为:2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O
答案:
(1)高锰酸钾制氧 氨气密度比空气小,易溶于水
(2)氨气极易溶于水,水会到吸入试管,将试管炸裂 增大氨气与水的接触面积,防止逸散到空气中,吸收的更彻底
(3)2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O
(1)制取氨气用的药品是氯化氨和消石灰固体,反应条件是加热,故发生装置应选高锰酸钾制氧气的装置;氨气密度比空气小,易溶于水,所以只能用向下排空气法收集;
(2)氨气极易溶于水,水会到吸入试管,将试管炸裂;为了防止其逸散到空气中污染空气,可以用水吸收,在出气管连接漏斗可增大氨气与水的接触面积,防止逸散到空气中,吸收的更彻底;
(3)实验室里通常用加热氯化铵固体和氢氧化钙固体混合物的方法制取氨气.其化学方程式为:2NH4Cl+Ca(OH)2
| ||
答案:
(1)高锰酸钾制氧 氨气密度比空气小,易溶于水
(2)氨气极易溶于水,水会到吸入试管,将试管炸裂 增大氨气与水的接触面积,防止逸散到空气中,吸收的更彻底
(3)2NH4Cl+Ca(OH)2
| ||
点评:气体的发生装置要看反应物的状态和反应条件:反应物是固体,反应条件是加热时,用固固加热型装置;气体的收集要看气体的密度和溶解性,氨气的密度比空气的密度小,并且极易溶于水,所以只能用向下排气法收集.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
当水分不蒸发,温度不改变,溶液放置较长时间后,溶质会( )
| A、沉降下来 | B、不会分离出来 |
| C、会浮出水面 | D、无法确定 |
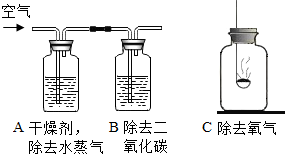 某学习小组选择从空气中制取氮气作为研究课题,以下是他们设计的实验方案:空气→除去水蒸气→除去二氧化碳→除去氧气→氮气
某学习小组选择从空气中制取氮气作为研究课题,以下是他们设计的实验方案:空气→除去水蒸气→除去二氧化碳→除去氧气→氮气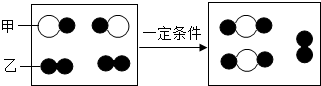
 ”聚集成的物质
”聚集成的物质