题目内容
7.20g黄铜(铜锌合金)加入装有200g稀硫酸的烧杯中,恰好完全反应,待不再产生气体时烧杯中质量减少0.4g.请计算:(1)黄铜中铜的质量分数.
(2)反应后所得溶液中的溶质质量分数.
分析 铜不能和稀硫酸反应,锌和稀硫酸反应生成硫酸锌和氢气,不再产生气体时烧杯中质量减少0.4g,说明反应生成了0.4g氢气;
根据氢气的质量可以计算锌的质量和生成的硫酸锌的质量,进一步可以计算黄铜中铜的质量分数和反应后所得溶液中的溶质质量分数.
解答 解:设锌的质量为x,生成硫酸锌的质量为y,
Zn+H2SO4═ZnSO4+H2↑,
65 161 2
x y 0.4g
$\frac{65}{x}$=$\frac{161}{y}$=$\frac{2}{0.4g}$,
x=13g,y=32.2g,
黄铜中铜的质量分数为:$\frac{20g-13g}{20g}$×100%=35%,
答:黄铜中铜的质量分数为35%.
(2)反应后所得溶液中的溶质质量分数为:$\frac{32.2g}{13g+200g-0.4g}$×100%=15.1%,
答:反应后所得溶液中的溶质质量分数为15.1%.
点评 计算溶液质量时,因为铜不能和稀硫酸反应,也不能溶于水,因此不能形成溶液的一部分,要注意理解.

练习册系列答案
相关题目
17.除去下列各物质中的少量杂质,所选用的试剂、方法均正确的是( )
| 物质 | 杂质(少量) | 加入试剂及用量 | 除杂操作方法 | |
| A | KCl 溶液 | CaCl2 | 适量的Na2C03溶液 | 过滤,除去滤渣 |
| B | NaOH | Na2C03 | 过量的盐酸 | 加热蒸发 |
| C | Cu(NO3)2 | AgNO3 | 过量的铜粉 | 过滤 |
| D | CO | CO2 | 足量的氧化铜 | 加热 |
| A. | A | B. | B | C. | C | D. | D |
18.化学中元素符号能表示一定的意义,不同的元素符号表示的意义不同.下列对元素符号表示的意义解释正确的是( )
| 序号 | 元素符号 | 元素符号所表示的意义 |
| A | H | 只表示氢元素 |
| B | Fe | 表示铁元素,表示一个铁原子,表示铁这种物质 |
| C | N | 只表示一个氮原子 |
| D | O | 表示氧元素,表示一个氧原子,表示氧气这种物质 |
| A. | A | B. | B | C. | C | D. | D |
12.下列溶液pH最小的是( )
| A. | 20% KOH | B. | 10% KOH | C. | 20% HCl | D. | 10% HCl |
16.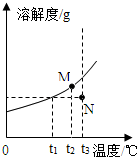 如图为A物质的溶解度曲线.M、N两点分别表示A物质的两种溶液.下列做法不能实现M、N间的相互转化的是(A从溶液中析出时不带结晶水)( )
如图为A物质的溶解度曲线.M、N两点分别表示A物质的两种溶液.下列做法不能实现M、N间的相互转化的是(A从溶液中析出时不带结晶水)( )
 如图为A物质的溶解度曲线.M、N两点分别表示A物质的两种溶液.下列做法不能实现M、N间的相互转化的是(A从溶液中析出时不带结晶水)( )
如图为A物质的溶解度曲线.M、N两点分别表示A物质的两种溶液.下列做法不能实现M、N间的相互转化的是(A从溶液中析出时不带结晶水)( )| A. | 从N→M:先向N中加入适量固体A再降温到t2 | |
| B. | 从N→M:先将N降温到t1再加入适量固体A | |
| C. | 从M→N:先将M降温到t1再将其升温 | |
| D. | 从M→N:先将M升温到t3再加入适量的水 |
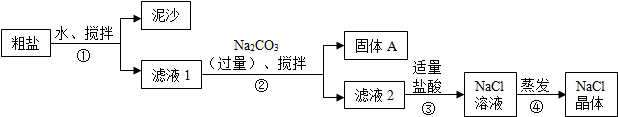
17.下列是“粗盐中难溶性杂质的去除”实验操作图,其中不正确的是( )
| A. |  称取5.0g粗盐 | B. |  量取10mL水 量取10mL水 | ||
| C. |  过滤 | D. |  蒸发 |
 铁是应用最广泛的金属.据估计,每年全世界被腐蚀损耗的钢铁材料,约占全年钢产量的十分之一.
铁是应用最广泛的金属.据估计,每年全世界被腐蚀损耗的钢铁材料,约占全年钢产量的十分之一.


