题目内容
20.有一种生活中常见的液态燃料,现在取这种燃料2.3g在足量氧气中充分燃烧,生成4.4g二氧化碳和2.7g水,则你认为该燃料的组成为( )| A. | 一定含碳、氢、氧三种元素 | B. | 一定含碳、氢元素,可能含氧元素 | ||
| C. | 一定含碳、氢元素,不含氧元素 | D. | 无法确定 |
分析 根据质量守恒定律,反应前后元素种类、质量不变,由生成二氧化碳和水的量分别计算出可燃物中C和H元素质量.然后比较所求C、H元素质量和与可燃物质量是否相等,若相等可燃物就只含C、H两种元素,若不等可燃物中还含有O元素.
解答 解:生成的4.4g二氧化碳和2.7g水中C、H元素质量分别为:
C元素质量:4.4g×$\frac{12}{44}$×100%=1.2g;H元素质量:2.7g×$\frac{2}{18}$×100%=0.3g;
C、H元素质量和=1.2g+0.3g=1.5g;
∵1.5g<2.3g,∴可燃物中除C、H元素外还含O元素;
故选A.
点评 此类问题的变化就在于可燃物质量是否已知,不说明可燃物的质量时,只能得到可燃物一定含C、H元素可能含O元素的结论;在可燃物质量明确时,是否含O元素就可以得到确定的结论

练习册系列答案
 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案
相关题目
10.下列关于分子、原子、离子的说法正确的是( )
| A. | 分子总比原子大 | |
| B. | 分子不带电,原子、离子都带电 | |
| C. | 分子、原子、离子都能构成物质 | |
| D. | 一切原子的原子核都是由质子、中子构成的 |
12.用分子的观点对下列现象的解释,其中错误的( )
| A. | 湿衣服晾干--------分子在不断运动 | |
| B. | 水受热变成水蒸气-------分子间有间隙 | |
| C. | 食物腐败--------分子本身发生变化 | |
| D. | 热胀冷缩--------分子大小随温度改变而改变 |
9.鱼油中富含的DHA(C22H32O2)是大脑细胞形成和发育不可缺少的物质,下列关于DHA的叙述中不正确的是( )
| A. | DHA由碳、氢、氧三种元素组成 | |
| B. | DHA由C22H32O2分子构成 | |
| C. | DHA由22个碳原子、32个氢原子、2个氧原子构成 | |
| D. | DHA属于化合物 |

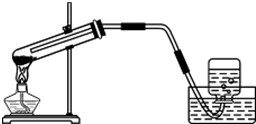 我县一所初中的化学兴趣小组的同学利用如图所示装置进行利用分解高锰酸钾制取氧
我县一所初中的化学兴趣小组的同学利用如图所示装置进行利用分解高锰酸钾制取氧