题目内容
18.钠的化合物在日常生活中应用广泛.(1)NaOH溶液常用于鸡舍消毒,请写出NaOH的俗称是烧碱(任写一个).
(2)次氯酸钠(NaClO)是“84”消毒液的有效成分,次氯酸钠中氯元素的化合价是+1价.
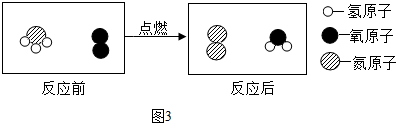
(3)碳酸氢钠是发酵粉的有效成分,碳酸氢钠与稀盐酸反应的化学方程式为NaHCO3+HCl=NaCl+CO2↑+H2O.
(4)从微观视角看物质的变化是化学特有的思维方式.下面三幅示意图分别表示生成氯化钠的不同化学反应.请根据图示回答相关问题:
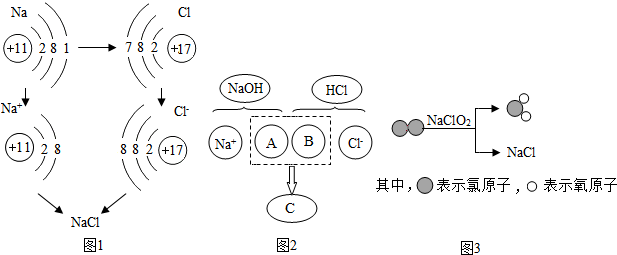
①图1是金属钠与氯气反应生成氯化钠的微观示意图.由图1可知,元素的化学性质与A(填字母序号)有密切关系.
A.最外层电子数 B.内层电子数 C.电子层数
②图2描述了NaOH溶液与盐酸反应的微观实质,图中A、C处应填入的离子符号或化学式依次为OH-、H2O.
③图3表示反应的化学方程式为Cl2+NaClO2=ClO2+NaCl.
分析 (1)氢氧化钠俗称烧碱、火碱、苛性钠;
(2)在化合物中各元素正负化合价的代数和为零;
(3)根据碳酸氢钠与酸反应的反应原理写出化学方程式;
(4)根据酸碱反应的实质以及物质的构成微粒解答即可.
解答 解:(1)氢氧化钠俗称烧碱、火碱、苛性钠,故填:烧碱;
(2)根据化合物中各元素正负化合价的代数和为零,化合物中钠元素的化合价是+1价,氧元素的化合价是-2价,设氯元素的化合价为x,则有(+1)+x+(-2)=0,解得x=+1,故填:+1;
(3)碳酸氢钠能与盐酸反应生成氯化钠、水和二氧化碳,方程式是NaHCO3+HCl=NaCl+H2O+CO2↑,故填:NaHCO3+HCl=NaCl+H2O+CO2↑;
(4)①元素的化学性质与元素原子的最外层电子数有关,故填:A;
②氢氧化钠与盐酸的反应,实质是氢氧根离子和氢离子结合生成水的过程,故填:OH-、H2O;
③据图可以看出该反应是Cl2+NaClO2=ClO2+NaCl,故填:Cl2+NaClO2=ClO2+NaCl.
点评 本题考查了常见物质的俗称以及有关物质的构成和方程式的书写的知识,完成此题,可以依据已有的知识进行分析解答.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.下列有关化学知识的说法正确的是( )
| A. | A向某未知溶液中滴入Ba(OH)2溶液,产生白色沉淀后滴入足量HNO3,若沉淀不溶解由原溶液中一定含有SO42- | |
| B. | 用HCl溶液可区别AgNO3、Na2CO3、NaCl三瓶无色溶液 | |
| C. | 除去NaCl少量的Na2SO4,加水溶解后加入适量的Ba(NO3)2溶液,然的过滤,蒸发 | |
| D. | 化学反应3X=Y+2Z中,若X的相对分子质量为M,Y的相对分子质量为N,则Z的相对分子质量为M-N |
13.下列有关实验现象的描述,错误的是( )
| A. | 红磷在空气中燃烧,产生大量白烟 | |
| B. | 向氢氧化钠溶液中滴入硫酸铜溶液生成蓝色沉淀 | |
| C. | 将红热的细铁丝放在氧气中,剧烈燃烧,火星四射,生成氧化铁黑色固体 | |
| D. | 硫在氧气中燃烧时,产生蓝紫色火焰,生成有刺激性气味的气体 |
3.下列实验现象的描述正确的是( )
| A. | 蜡烛在空气中燃烧生成二氧化碳和水 | |
| B. | 硫在空气中燃烧,发出明亮的蓝紫色火焰 | |
| C. | 红磷在空气中燃烧产生大量白色烟雾 | |
| D. | 铁丝在氧气中燃烧,火星四射,生成黑色固体,放出大量的热 |
10.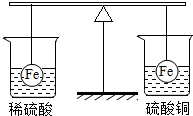 如图所示,在等臂杠杆的两端各系一只等质量等体积的铁球,这时杠杆平衡.然后将两球分别浸没在稀硫酸和硫酸铜溶液中片刻,下列说法正确的是( )
如图所示,在等臂杠杆的两端各系一只等质量等体积的铁球,这时杠杆平衡.然后将两球分别浸没在稀硫酸和硫酸铜溶液中片刻,下列说法正确的是( )
 如图所示,在等臂杠杆的两端各系一只等质量等体积的铁球,这时杠杆平衡.然后将两球分别浸没在稀硫酸和硫酸铜溶液中片刻,下列说法正确的是( )
如图所示,在等臂杠杆的两端各系一只等质量等体积的铁球,这时杠杆平衡.然后将两球分别浸没在稀硫酸和硫酸铜溶液中片刻,下列说法正确的是( )| A. | 左边烧杯中溶液质量减少 | B. | 右边烧杯中溶液的质量增加 | ||
| C. | 杠杆仍保持平衡 | D. | 杠杆向右倾斜 |
8.钙是人体中的常量元素,缺钙时可通过食用保健药剂来增加摄入量.某补钙药剂说明书的部分信息如图1所示.现将100g盐酸分成5等份,逐次加到用40片该药剂制成的粉末中(其他成分不与盐酸反应),得到部分数据与图象如表格及图2.请根据有关信息回答问题.

(1)a的数值为25.
(2)求该品牌补钙药剂中CaCO3的质量分数.
(3)求该盐酸中溶质的质量分数.(写出计算过程,计算结果保留一位小数)
| 第1次 | 第3次 | 第4次 | |
| 加入盐酸的质量(g) | 20 | 20 | 20 |
| 剩余固体的质量(g) | 35 | a | 20 |

(1)a的数值为25.
(2)求该品牌补钙药剂中CaCO3的质量分数.
(3)求该盐酸中溶质的质量分数.(写出计算过程,计算结果保留一位小数)