题目内容
孔雀石是冶炼金属铜的主要原料,其主要成分是Cu2(OH)2CO3〔可看成是Cu(OH)2?CuCO3〕,还含少量氧化铁和二氧化硅(不溶于水,也不与酸反应).以下为“湿法炼铜”并制备其它副产品氯化钠和铁红(氧化铁)的工业流程.

资料:1Cu2(OH)2CO3与盐酸反应生成氯化铜、水和二氧化碳气体;
2铁能与氯化铁溶液反应,反应方程式为2FeCl3+Fe═3FeCl2
3氢氧化亚铁易被氧气氧化,反应方程式为4Fe(OH)2+2H2O+O2═4Fe(OH)3
回答下列问题:
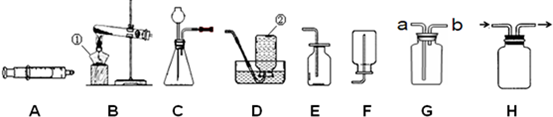
(1)实验室在获取NaCl晶体的操作Y中,使用的仪器有:铁架台、玻璃棒、酒精灯、 ;
(2)写出盐酸与氧化铁反应的化学方程式: ;
(3)在滤液Ⅰ中加入过量铁粉,搅拌至充分反应,其中发生的置换反应有 个;
(4)试剂X中溶质的化学式为 ;
(5)在洗涤、干燥获取铜粉时,洗涤的目的是 .

资料:1Cu2(OH)2CO3与盐酸反应生成氯化铜、水和二氧化碳气体;
2铁能与氯化铁溶液反应,反应方程式为2FeCl3+Fe═3FeCl2
3氢氧化亚铁易被氧气氧化,反应方程式为4Fe(OH)2+2H2O+O2═4Fe(OH)3
回答下列问题:
(1)实验室在获取NaCl晶体的操作Y中,使用的仪器有:铁架台、玻璃棒、酒精灯、
(2)写出盐酸与氧化铁反应的化学方程式:
(3)在滤液Ⅰ中加入过量铁粉,搅拌至充分反应,其中发生的置换反应有
(4)试剂X中溶质的化学式为
(5)在洗涤、干燥获取铜粉时,洗涤的目的是
考点:常见金属的冶炼方法,蒸发与蒸馏操作,酸的化学性质,置换反应及其应用,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:(1)根据蒸发结晶的实验来分析所用仪器;
(2)盐酸与氧化铁反应生成氯化铁和水;
(3)滤液是氯化铜溶液和盐酸的混合物,均能与铁发生置换反应;
(4)根据分离铜和铁的混合物的方法来分析;
(5)铜粉表面沾有其他物质.
(2)盐酸与氧化铁反应生成氯化铁和水;
(3)滤液是氯化铜溶液和盐酸的混合物,均能与铁发生置换反应;
(4)根据分离铜和铁的混合物的方法来分析;
(5)铜粉表面沾有其他物质.
解答:解:(1)溶液的蒸发结晶中需要用到酒精灯、铁架台、蒸发皿、玻璃棒等;
故填:蒸发皿;
(2)盐酸与氧化铁反应生成氯化铁和水,其化学方程式:6HCl+Fe2O3═2FeCl3+3H2O.
故填:6HCl+Fe2O3═2FeCl3+3H2O;
(3)在滤液Ⅰ中中含有氯化铜和氯化氢两种溶质,加入过量铁粉,铁能置换出氯化铜中的铜,还能与稀盐酸发生置换反应;
故填:两;
(4)固体B是铁粉和铜粉的混合物,分离开并得到氯化亚铁,需要加入稀盐酸.
故填:HCl;
(5)铜粉是从氯化亚铁溶液中过滤出来的,其表面沾有氯化亚铁,需要用水进行清洗.
故填:洗掉铜粉上附着的氯化亚铁溶液.
故填:蒸发皿;
(2)盐酸与氧化铁反应生成氯化铁和水,其化学方程式:6HCl+Fe2O3═2FeCl3+3H2O.
故填:6HCl+Fe2O3═2FeCl3+3H2O;
(3)在滤液Ⅰ中中含有氯化铜和氯化氢两种溶质,加入过量铁粉,铁能置换出氯化铜中的铜,还能与稀盐酸发生置换反应;
故填:两;
(4)固体B是铁粉和铜粉的混合物,分离开并得到氯化亚铁,需要加入稀盐酸.
故填:HCl;
(5)铜粉是从氯化亚铁溶液中过滤出来的,其表面沾有氯化亚铁,需要用水进行清洗.
故填:洗掉铜粉上附着的氯化亚铁溶液.
点评:在解此类题时,首先要熟悉题中设计的反应原理,然后结合反应原理和质量守恒定律判断化学式和书写方程式.

练习册系列答案
相关题目
以下操作可以达到实验目的是( )
| A、加水溶解并过滤除去CaO中的CaCO3 |
| B、用适量盐酸除去KCl溶液中混有的少量K2CO3 |
| C、用灼烧的方法除去铜粉中混有的少量木炭粉 |
| D、通入适量的氧气后点燃除去二氧化碳中少量一氧化碳气体 |
下列四个图象中,能正确表示对应变化关系的是( )
A、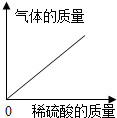 向一定量铁粉中加入稀硫酸 |
B、 一定温度下,向不饱和硝酸钾溶液中加入硝酸钾 |
C、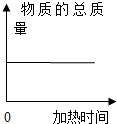 碳在密闭容器中(含空气)加热反应 |
D、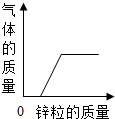 向一定量的稀硫酸和硫酸锌的混合溶液中加入锌粒 |
 能源与环境问题是当今社会备受关注的热点.
能源与环境问题是当今社会备受关注的热点.