题目内容
19. A-D是初中化学常见的物质,A、D是无色气体,B、C是黑色固体,A、C是单质,B、D化合物,它们之间有如图关系(“-”表示物质间能相互反应,“→”表示物质间的转化关系,部分反应物,生成物省略).请回答下列问题:D的化学式是CO.
A-D是初中化学常见的物质,A、D是无色气体,B、C是黑色固体,A、C是单质,B、D化合物,它们之间有如图关系(“-”表示物质间能相互反应,“→”表示物质间的转化关系,部分反应物,生成物省略).请回答下列问题:D的化学式是CO.
分析 根据A-D是初中化学常见的物质,A、D是无色气体,B、C是黑色固体,A、C是单质,B、D化合物,A会转化成B,所以B可以是氧化铜,A是氧气,C会与氧化铜反应,所以C是碳,C转化成的D会与氧气反应,所以D是一氧化碳,一氧化碳会与氧化铜反应,然后将推出的物质进行验证即可.
解答 解:A-D是初中化学常见的物质,A、D是无色气体,B、C是黑色固体,A、C是单质,B、D化合物,A会转化成B,所以B可以是氧化铜,A是氧气,C会与氧化铜反应,所以C是碳,C转化成的D会与氧气反应,所以D是一氧化碳,一氧化碳会与氧化铜反应,经过验证,推导正确,所以D是CO.
故答案为:CO.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

练习册系列答案
 优生乐园系列答案
优生乐园系列答案
相关题目
10.下列有关说法中,错误的是( )
| A. | 原子中原子核与核外电子的电量相等,电性相反,所以整个原子不显电性 | |
| B. | 水通电产生氢气和氧气,说明水中含有氢分子和氧分子 | |
| C. | 分子原子离子都能直接构成物质 | |
| D. | 不同元素最本质的区别在于相对原子质量不同 |
7. 某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.
某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.
(1)请写出镁条与氧气反应的化学方程式2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO.
(2)小明发现燃烧产物的质量大于反应物镁条的质量,认为这个反应不遵守质量守恒定律,我不同意(填“同意”或“不同意”)小明的观点,因为所有的化学反应都遵循质量守恒定律.
(3)小明在实验中发现镁条的燃烧产物中还有少量黄色固体.
提出问题:黄色固体是什么呢?
查阅资料:①氧化镁为白色固体;
②镁能与氮气反应生成黄色的氮化镁固体;
③氮化镁可与水剧烈反应生成氨气,该气体能使湿润的红色石蕊试纸变蓝.
做出猜想:黄色固体为氮化镁固体(化学式为Mg3N2).
实验探究:请设计实验,验证猜想.
反思与交流:空气中氮气的含量远大于氧气的含量,而镁条在空气中燃烧生成的白色氧化镁却远多于黄色氮化镁,为什么呢?请给出合理的解释氧气的化学性质比氮气更活泼,镁条更容易与氧气发生反应.
 某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.
某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.(1)请写出镁条与氧气反应的化学方程式2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO.
(2)小明发现燃烧产物的质量大于反应物镁条的质量,认为这个反应不遵守质量守恒定律,我不同意(填“同意”或“不同意”)小明的观点,因为所有的化学反应都遵循质量守恒定律.
(3)小明在实验中发现镁条的燃烧产物中还有少量黄色固体.
提出问题:黄色固体是什么呢?
查阅资料:①氧化镁为白色固体;
②镁能与氮气反应生成黄色的氮化镁固体;
③氮化镁可与水剧烈反应生成氨气,该气体能使湿润的红色石蕊试纸变蓝.
做出猜想:黄色固体为氮化镁固体(化学式为Mg3N2).
实验探究:请设计实验,验证猜想.
| 实验操作 | 实验现象 | 结论 |
| 取少量黄色固体于试管中,加入适量的水,并将湿润的红色石蕊试纸放在试管口. | 试管中有气体产生,湿润的红色石蕊试纸变蓝 | 猜想正确 |
7.小亮同学实验测得的下列数据中,合理的是( )
| A. | 用烧杯量取48.2mL水 | |
| B. | 用量程为100mL的量筒量取90mL氯化钠溶液 | |
| C. | 用托盘天平称得某固体样品的质量为8.15g | |
| D. | 用体温计测得自己的体温为37.22摄氏度 |
4.小明在量取液体体积时,他首先将量筒放平,俯视液面读数为45mL,然后他将液体倒出一部分,由于匆忙再次俯视读数为23mL,则小明实际倒出的液体体积为( )
| A. | 无法确定 | B. | 大于22mL | C. | 小于22mL | D. | 22mL |
5.除去下列各物质中的少量杂质,所选用的试剂及操作方法均正确的是( )
| 选项 | 物质(括号内为杂质) | 试剂 | 操作方法 |
| A | CO2(CO) | 足量O2 | 点燃 |
| B | NaCl(NaOH) | 过量的稀盐酸 | 蒸发结晶 |
| C | HCl(CO2) | 适量NaOH溶液 | 洗气 |
| D | 稀盐酸(稀硫酸) | 适量硝酸钡溶液 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
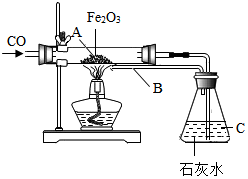 有位同学设计了下列实验(装置及所用药品如图所示),仔细观察后回答下列问题.
有位同学设计了下列实验(装置及所用药品如图所示),仔细观察后回答下列问题.