题目内容
现有6g镁分别与不同质量的氧气反应,试将生成氧化镁的质量填入下表并通过计算回答下列问题:
(1)第一次试验中,6g镁和2g的氧气反应为什么不能生成8g的氧化镁?
(2)第二次试验以后,为什么不断增加氧气的质量,生成MgO的质量却不增加?
| 氧气的质量/g | 生成MgO的质量/g |
| 2 | |
| 4 | |
| 8 | |
| 12 |
(2)第二次试验以后,为什么不断增加氧气的质量,生成MgO的质量却不增加?
考点:根据化学反应方程式的计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:利用镁在氧气中燃烧的化学方程式,求出6g镁完全反应需氧气的质量,然后根据图示数据进行分析,即可得出每次实验生成氧化镁的质量;据此即知第几次氧气过量,第几次镁过量;根据完全反应的概念,结合计算出的数据分析虽然氧气的量不断增加,但是生成的氧化镁的质量却不再增加的原因
解答:解:6g镁完全反应,需氧气的质量为x,
2Mg+O2
2MgO
48 32
6g x
=
x=4g
6g镁完全反应,需氧气的质量为4g,根据质量守恒定律,生成氧化镁的质量=6g+4g=10g;
①当氧气的质量为2g,需要硫的质量为3g,硫有剩余,没有完全参加化学反应,故不能生成8g的氧化镁,生成氧化镁的质量=2g+3g=5g;
②6g镁与4g氧气完全反应,生成氧化镁的质量=4g+6g=10g;
6g镁完全反应,需氧气的质量为4g,故③④中氧气有剩余,生成氧化镁的质量=10g.
答案:
(1)镁有剩余,没有完全参加化学反应,故不能生成8g的氧化镁;
(2)因为第二次镁已反应完,反应不再进行,故生成的氧化镁的质量不再增加.
2Mg+O2
| ||
48 32
6g x
| 48 |
| 6g |
| 32 |
| x |
x=4g
6g镁完全反应,需氧气的质量为4g,根据质量守恒定律,生成氧化镁的质量=6g+4g=10g;
①当氧气的质量为2g,需要硫的质量为3g,硫有剩余,没有完全参加化学反应,故不能生成8g的氧化镁,生成氧化镁的质量=2g+3g=5g;
②6g镁与4g氧气完全反应,生成氧化镁的质量=4g+6g=10g;
6g镁完全反应,需氧气的质量为4g,故③④中氧气有剩余,生成氧化镁的质量=10g.
答案:
| 氧气的质量/g | 生成MgO的质量/g |
| 2 | 5 |
| 4 | 10 |
| 8 | 10 |
| 12 | 10 |
(2)因为第二次镁已反应完,反应不再进行,故生成的氧化镁的质量不再增加.
点评:本题是有关化学方程式的简单计算.解题的关键是求出6g镁完全反应需氧气的质量.

练习册系列答案
相关题目
自2004年5月1日我国“道路交通安全法”实施以来,交管部门进一步强化了对司机酒后开车的监控处罚力度.交警常用装有重铬酸钾的仪器检测司机是否酒后开车,因为乙醇分子等可以使橙红色的重铬酸钾变为绿色的硫酸铬.重铬酸钾(K2Cr2O7)中,铬元素的化合价为( )
| A、+6 | B、+3 | C、-5 | D、+5 |
下列化学现象的描述,正确的是( )
| A、红磷在空气中不能燃烧 |
| B、硫在氧气中燃烧,发出蓝紫色火焰 |
| C、铁在空气中剧烈燃烧,火星四射,生成黑色固体,发热 |
| D、红磷在氧气中燃烧生成一种白色气体 |
2004年5月1日实施的新交通法加大了对“酒后驾车”的处罚力度.交警常用装有重铬酸钾(K2Cr2O7)的仪器,检测司机是否酒后驾车.其原理是红色的重铬酸钾遇酒精后生成蓝绿色物质.下列说法不正确的是( )
| A、该变化为化学变化 |
| B、重铬酸钾中铬元素的化合价为+3 |
| C、分子是不断运动的 |
| D、酒精具有挥发性 |
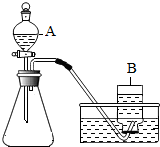 在实验室里,常用分解过氧化氢溶液、加热氯酸钾或高锰酸钾制取氧气.某化学兴趣小组对氧气的实验室制法进行了探究.
在实验室里,常用分解过氧化氢溶液、加热氯酸钾或高锰酸钾制取氧气.某化学兴趣小组对氧气的实验室制法进行了探究.