题目内容
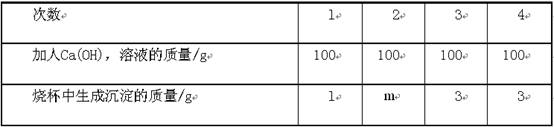
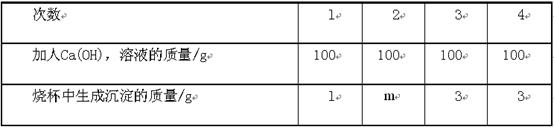
(6分)实验室中有一瓶存放时间过长的NaOH药品,其中一部分已转化为Na2C03。取lOg该药品放入烧杯中,加154g水配成溶液,将400g一定溶质质量分数的Ca(0H)2溶液分四次加人该烧杯中,充分反应后,测得生成沉淀质量的数据记录如下表:

(1)m=____g,
(2)求10g该药品中Na2C03的质量,
(3)第三次加入Ca(OH)2溶液充分反应后,所得溶液中溶质质量分数是多少?
(1)2
(2)解:根据题意知共生成CaCO3的质量为3g
设10g药品中含Na2CO3的质量为 X,同时生成 NaOH的质量为Y
Na2CO3 + Ca(OH)2 == CaCO3↓+ 2NaOH
106 100 80
X 3 y
106/X=100/3=80/Y
X=3.18g Y=2.4g
(3)第三次反应后溶质NaOH 的质量=10-3.18+2.4=9.22g
第三次反应后溶液质量=154+10+300-3=461g
NaOH的质量分数为9.22/461ⅹ100%=2%
答:10g药品中含Na2CO3的质量为3.18g, 第三次反应后溶液中溶质质量分数2%。
【解析】略

 名校课堂系列答案
名校课堂系列答案(1)实验室中有一瓶敞口放置的浓盐酸。它的质量分数和放置天数的关系如图1。假设水不蒸发,分析浓盐酸的溶质质量分数变化的原因 。
(2)观察图2,向小试管内滴加水后,可观察到的现象是 。解释产生此现象的原因 。
 |
(3)图3图4分别是溴化氢(HBr)和乙醇(C2H5OH)在水中的微观示意图。请你结合已有的酸、碱知识,判断溴化氢的水溶液显 (填“酸性”、“中性”或“碱性”下同),乙醇的水溶液显 。
(4)向盛有10mL稀盐酸(其中滴有少量指示剂)的烧杯中加入氢氧化钠溶液,用pH计测定溶液的pH,所得数据如下。请分析并回答下列问题:
| 加入NaOH溶液的体积/mL | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 |
| 烧杯中溶液的pH | 1.1 | 1.2 | 1.4 | 1.6 | 2.5 | 7.0 | 11.0 | 12.0 |
①写出稀盐酸和氢氧化钠溶液反应的化学方程式 。
②若滴加的指示剂是紫色石蕊溶液,当加入氢氧化钠溶液的体积为13mL时,溶液显 色。
③若滴加的指示剂是无色酚酞溶液,加入氢氧化钠溶液充分振荡后,溶液颜色无变化。此时溶液中的溶质一定有(填化学式) 。