题目内容
14.某课外小组的同学收集了含水蒸气、一氧化碳和二氧化碳的废气,为确认这种废气中存在CO,他们在实验室按人图所示装置进行实验〔气体通过装置A速度很慢,假设在此处发生的反应完全;碱石灰(CaO和NaOH的混合物)过量〕.
(1)A中碱石灰的作用是除去废气中的水和二氧化碳.
(2)B中发生反应的化学方程式是3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(3)该实验能证明混合气体中存在CO的现象是B中红色粉末变黑、C中石灰水有气泡产生且变浑浊.
(4)D中酒精灯的作用是处理尾气.
分析 (1)碱石灰能够吸收水和二氧化碳;
(2)根据反应物和生成物及其质量守恒定律可以书写化学方程式;
(3)氧化铁和一氧化碳在高温条件下反应能生成铁和二氧化碳;
(4)CO有毒,需要处理.
解答 解:(1)A中碱石灰的作用是除去废气中的水和二氧化碳.
故填:除去废气中的水和二氧化碳.
(2)B中发生反应的化学方程式是:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
故填:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(3)该实验能证明混合气体中存在CO的现象是B中红色粉末变黑;C中石灰水有气泡产生且变浑浊.
故填:B中红色粉末变黑、C中石灰水有气泡产生且变浑浊.
(4)一氧化碳还原氧化铁实验中,由于一氧化碳是有毒的气体,故酒精灯起到了处理尾气的作用,
故填:处理尾气.
点评 解答本题要掌握化学方程式的书写方法,同时要充分理解物质之间相互作用时的实验现象,只有这样才能对问题做出正确的判断.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.“可燃冰”是一种未来的清洁能源.现已探明,我国南海海底有极丰富的甲烷资源.据报道,这些蕴藏在海底的甲烷在高压下形成象冰一样的甲烷水合物(化学式为CH4•8H2O),它又称“可燃冰”.以下说法中不正确的是( )
| A. | “可燃冰”的可燃成分是甲烷 | |
| B. | “可燃冰”的相对分子质量是160 | |
| C. | “可燃冰”提供了水可能变成油的证据 | |
| D. | 甲烷水合物是由三种元素构成的纯净物 |
2.化学在能源、材料和环境等研究领域发挥着重要作用.下列说法不正确的是( )
| A. | 二氧化碳、甲烷和淀粉都属于有机物 | |
| B. | 石油、煤和天然气都是不可再生能源 | |
| C. | 合金是一种混合物,它可以看成是一种溶液 | |
| D. | 太阳能、风能和地热能的利用都有利于保护环境 |
19.除去粗盐中的难溶性杂质的主要步骤有:①过滤②蒸发③溶解.下列操作顺序正确的是( )
| A. | ①②③ | B. | ②③① | C. | ③①② | D. | ②①③ |
4.工业上利用乙炔(C2H2)产生的灰浆和残渣制备化工原料KClO3和超细CaCO3.
生产流程为:电石(CaC2)$\stackrel{水}{→}$灰浆$\stackrel{置露于空气}{→}$残渣.
资料:电石与水的反应为:CaC2+2H2O=Ca(OH)2+C2H2↑.
(1)残渣中主要成分是Ca(OH)2和CaCO3.
Ⅰ.制备KClO3的流程如下:
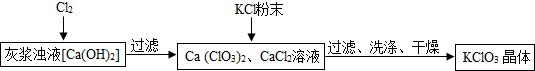
(2)向灰浆浊液中通入Cl2,得到Ca(ClO3)2、CaCl2溶液.反应中Ca(ClO3)2与CaCl2的化学计量数分别为1和5.写出此反应的化学方程式6Ca(OH)2+6Cl2=Ca(ClO3)2+5CaCl2+6H2O.
(3)有关物质在常温下的溶解度如下:
上述流程中加入KCl粉末,KCl与Ca(ClO3)2(填化学式)发生了复分解反应,得到KClO3晶体.你认为能得到KClO3晶体的原因是相同温度下,氯酸钾的溶解度小.
(4)洗涤时,可选用下列BC洗涤剂(填字母编号).
A、KCl饱和溶液 B、冰水 C、饱和KClO3溶液
Ⅱ.制备超细CaCO3的流程如下(注:加入NH4Cl的目的是溶解残渣中的难溶盐):
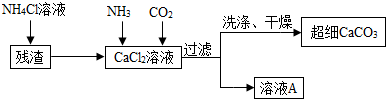
(5)流程中溶液A可循环使用,其主要成分的化学式是NH4Cl.
生产流程为:电石(CaC2)$\stackrel{水}{→}$灰浆$\stackrel{置露于空气}{→}$残渣.
资料:电石与水的反应为:CaC2+2H2O=Ca(OH)2+C2H2↑.
(1)残渣中主要成分是Ca(OH)2和CaCO3.
Ⅰ.制备KClO3的流程如下:

(2)向灰浆浊液中通入Cl2,得到Ca(ClO3)2、CaCl2溶液.反应中Ca(ClO3)2与CaCl2的化学计量数分别为1和5.写出此反应的化学方程式6Ca(OH)2+6Cl2=Ca(ClO3)2+5CaCl2+6H2O.
(3)有关物质在常温下的溶解度如下:
| 物质 | Ca(ClO3)2 | CaClO3 | KClO3 | KCl |
| 溶解度/g | 209.0 | 74.5 | 7.3 | 34.2 |
(4)洗涤时,可选用下列BC洗涤剂(填字母编号).
A、KCl饱和溶液 B、冰水 C、饱和KClO3溶液
Ⅱ.制备超细CaCO3的流程如下(注:加入NH4Cl的目的是溶解残渣中的难溶盐):

(5)流程中溶液A可循环使用,其主要成分的化学式是NH4Cl.