题目内容
(6分) 用化学用语填空。
(1)2个氮分子______ ; (2)硫酸根离子____;
(3)+2价的铁元素_______;(4)碳酸钠_______(5)铜元素___________
(6)天然气的主要成分的化学式___________
(1) 2N2 ;(2) SO42-;(3)  (4) Na2CO3 ;(5)Cu;(6) CH4
(4) Na2CO3 ;(5)Cu;(6) CH4
【解析】(1)表示分子个数,在化学式前面加数字,故两个氮分子:2N2 ;(2) 离子符号表示方法:在元素符号右上角标明电性和电荷数,数字在前,符号在后,表示离子个数,直接在离子符号前面加数字。故三个硫酸根离子表示为:SO42-;(3)化合价的表示方法:在元素符号正上方标出化合价.符号在前,数字在后,故+2价的镁元素表示为: ;(4)碳酸钠的化学式表示为:Na2CO3 ;(5)铜元素用元素符号表示为:Cu;(6)天然气的主要成分是甲烷,其化学式为:CH4
;(4)碳酸钠的化学式表示为:Na2CO3 ;(5)铜元素用元素符号表示为:Cu;(6)天然气的主要成分是甲烷,其化学式为:CH4
试题分析:根据表示多个分子就是在其化学式前加数字分析;根据离子的表示方法是在表示该离子的元素符号或原子团的右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略,分析;根据标在元素符号正上方的数字表示该元素化合价;根据铁在氧气中燃烧的产物是四氧化三铁;根据天然气的主要成分是甲烷,碳酸钠是由钠离子和碳酸根离子构成,结合化学式的书写方法书写其化学式;根据元素用元素符号表示分析.
考点:化学用语的意义和书写方法
点评:本题主要考查学生对化学用语的书写和理解能力,掌握化学符号的意义以及元素符号周围数字的意义是解答本题的关键,本题注重基础,题目难度不大.

 阅读快车系列答案
阅读快车系列答案研究性学习小组选择“H2O2生成O2的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:
【假设】 H2O2生成O2的快慢与催化剂种类有关
【实验方案】常温下,在两瓶相同体积的H2O2溶液中分别加入相同质量MnO2和红砖粉,测量各生成一瓶(相同体积)O2所需要的时间。
【进行实验】右下图是他们进行实验的装置图,此实验中B处宜采用的气体收集方法是: __________________。
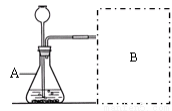
【实验记录】
实验编号 | 1 | 2 |
反应物 | 6% H2O2 | 6% H2O2 |
催化剂 | 1g 红砖粉 | 1g MnO2 |
时间 | 152 s | 35 s |
【结论】该探究过程得出的结论是_______________________________________________。
【反思】H2O2在常温下分解缓慢,加入MnO2或红砖粉后反应明显加快,若要证明MnO2和红砖粉是该反应的催化剂,还需要增加实验来验证它们在化学反应前后的_____________和_____________是否改变。


 意义的示意图是
意义的示意图是
