题目内容
将一定量的石灰石放入烧杯中,加入一定量的稀盐酸,恰好完全反应,产生4.4g气体,反应后所得溶液的溶质的质量分数为20%.(杂质不溶于水,也不参与反应)计算:反应前稀盐酸的溶质的质量分数.(结果精确到0.1%)
试题分析:设生成CaCl2的质量为x,石灰石中CaCO3的质量为y,参与反应的HCl的质量为z. CaCO3+2HCl=CaCl2+H2O+CO2↑ 100 73 111 44y z x 4.4g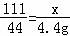 x=11.1g
x=11.1g 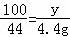 y="10" g
y="10" g 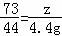 z=7.3g 所以反应后溶液的质量=
z=7.3g 所以反应后溶液的质量=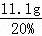 =55.5g反应前稀盐酸的溶质的质量分数=
=55.5g反应前稀盐酸的溶质的质量分数=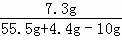 ×100%="14.6%"答:反应前稀盐酸的溶质的质量分数为14.6%.
×100%="14.6%"答:反应前稀盐酸的溶质的质量分数为14.6%.

练习册系列答案
相关题目