题目内容
4.通过对化学的学习,你已经掌握了实验室制取气体的有关规律,请结合如图回答问题:
(1)写出图中标号仪器的名称②锥形瓶,③长颈漏斗.
(2)用加热高锰酸钾的方法制取氧气,应选用发生装置和收集装置分别是A与D或F (填编号).某同学用B装置制取氧气,则发生反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(3)用C装置制取二氧化碳气体,检验二氧化碳气体是否收集满的方法是将燃着的木条放在集气瓶口,木条熄灭则满.
分析 (1)熟记仪器的名称;
(2)根据氧气的实验室制法以及发生装置和收集装置的选择条件即可;
(3)根据二氧化碳的性质来分析.
解答 解:(1)②是锥形瓶;③是长颈漏斗;故填:锥形瓶;长颈漏斗;
(2)加热高锰酸钾制取氧气的发生装置属于固体和固体加热制取气体,氧气不溶于水,可以采用排水法收集,同时密度比空气大,可以采用向上排空气法收集,B装置属于固体和液体不加热制取氧气,是用过氧化氢在二氧化锰的催化作用下分解为水和氧气.故填:A与D或F;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(3)检验二氧化碳是否收集满的方法是:用一根燃着的木条放在集气瓶口,若火焰熄灭,则证明瓶内气体已满;故填:将燃着的木条放在集气瓶口,木条熄灭则满.
点评 本题考查学生实验室制取氧气和二氧化碳的方法及操作步骤的知识,并学以致用.

练习册系列答案
相关题目
15.溶液与人类生活息息相关,溶液的配制是日常生活和化学实验中常见的操作,表是硫酸溶液和氨水的密度与其溶质质量分数对照表(20℃)
(1)氨水的密度与溶液中溶质质量分数的关系是氨水的密度随着溶液中溶质的质量分数的增大而减小;
(2)向10g28%的硫酸溶液中加水60g,摇匀,所得溶液的体积约是68.6mL(保留一位小数)
| 溶液中溶质的质量分数/% | 4 | 12 | 16 | 24 | 28 |
| 硫酸溶液的密度/g/cm3 | 1.02 | 1.08 | 1.11 | 1.17 | 1.20 |
| 氨水的密度/g/cm3 | 0.98 | 0.95 | 0.94 | 0.91 | 0.90 |
(2)向10g28%的硫酸溶液中加水60g,摇匀,所得溶液的体积约是68.6mL(保留一位小数)
9.下列各组物质间的反应,要借助酸碱指示剂才能判断出反应发生的是( )
| A. | 锌和稀盐酸 | B. | 烧碱溶液和稀硫酸 | ||
| C. | 氧化铁和稀硫酸 | D. | 硫酸铜溶液和铁 |
16.人们在如图所示的活动或操作过程中,发生化学变化的是( )
| A. | 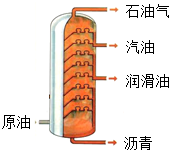 石油分馏 | B. | 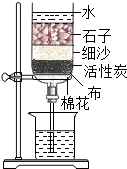 净化水 | ||
| C. | 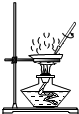 蒸发食盐水 | D. |  铁丝在氧气中燃烧 |
14.我国历史上爆发了有名的“鸦片战争”,鸦片屡禁不止,是由于易于吸食上瘾,其可能原因是( )
| A. | 鸦片味道好,是著名的美味剂 | |
| B. | 人由于心理失去平衡,追求某种特殊剌激 | |
| C. | 鸦片中存在的吗啡的分子结构与人脑中的分泌物脑肽的分子结构相近 | |
| D. | 生成鸦片的花罂粟很美 |


 ,该元素原子核内有6个质子,最外层有4个电子.该元素形成的两种最常见的单质是金刚石、石墨;这两种物质的物理性质差异很大,原因是碳原子间的排列方式不同.
,该元素原子核内有6个质子,最外层有4个电子.该元素形成的两种最常见的单质是金刚石、石墨;这两种物质的物理性质差异很大,原因是碳原子间的排列方式不同.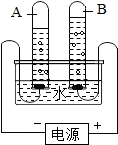 电解水的实验,如图装置,会带下列问题:
电解水的实验,如图装置,会带下列问题: