题目内容
17.用金属锌和铜的混合物100克与盐酸反应制取2克的氢气,请问该混合物中锌的质量是多少?分析 根据铜和锌的性质可知,加入稀盐酸时,只有锌与盐酸反应生成氯化锌和氢气;由生成氢气的质量,根据反应的化学方程式列式计算出参加反应锌的质量.
解答 解:设样品中锌的质量为x,
Zn+2HCl═ZnCl2+H2↑
65 2
x 2g
$\frac{65}{x}=\frac{2}{2g}$
x=65g
答:混合物中锌的质量是65g.
点评 本题难度不大,掌握化学方程式与溶质质量分数的综合计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
相关题目
16.化学家在环境问题上提出的最新构想是变废为宝,资源循环利用.例如 将燃料进行如下循环:这样既可解决能源问题,又能消除污染.上述构想中两个转化过程的变化为( )
燃料$\stackrel{(1)燃烧}{→}$ 燃烧产物 $\stackrel{(2)太阳能或生物能}{→}$燃料.
燃料$\stackrel{(1)燃烧}{→}$ 燃烧产物 $\stackrel{(2)太阳能或生物能}{→}$燃料.
| A. | (1)为物理变化,(2)为化学变化 | B. | 均为化学变化 | ||
| C. | (1)为化学变化,(2)为物理变化 | D. | 均为物理变化 |
2.下列实验操作正确的是( )
| A. | 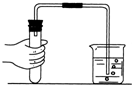 检验仪器气密性 检验仪器气密性 | B. | 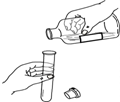 倾倒液体 | C. | 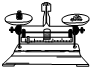 称量固体质量 | D. | 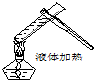 给液体加热 |
9.右图是某化工厂生产的产品包装袋上的标签.
(1)计算碳酸氢铵中各元素的原子个数比.
(2)计算碳酸氢铵的相对分子质量
(3)某农民李大伯需向自己的责任田中追施氮元素8.4kg;需这种氮肥多少千克?
(4)通过计算判断此产品是否是合格产品?
| 碳酸氢铵 化学式:NH4HCO3 含氮量:16.8% 纯度:95% 净重:50 kg |
(2)计算碳酸氢铵的相对分子质量
(3)某农民李大伯需向自己的责任田中追施氮元素8.4kg;需这种氮肥多少千克?
(4)通过计算判断此产品是否是合格产品?
6.过氧化氢(H2O2)常用作氧化剂、漂白 剂和消毒剂.为了贮存、运输、使用的方便,工业上将过氧化氢转化为固态的过碳酸钠晶体(2Na2CO3•3H2O2),该晶体具有碳酸钠和过氧化氢的双重性质.接触下列物质不会使过碳酸钠失效的是( )
| A. | 二氧化锰 | B. | 熟石灰 | C. | 盐酸 | D. | 氯化钠 |
7.2011年3月11日13时46分,日本9级特大地震引发福岛第一核电站爆炸,放射性物质的扩散问题牵动全世界人们的心.福岛核电站使用的是“铀钚混合型燃料”.下列说法中正确的是( )
| A. | 核泄漏对人类的生存影响大,因此必须立即关闭世界上所有的核电站 | |
| B. | 核电站中铀转变为钚是化学变化 | |
| C. | 铀的原子序数是92,铀的相对原子质量为92 | |
| D. | 铀与氧气化合生成UO3,该化合物中铀的化合价为+6价 |