题目内容
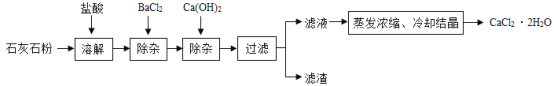
【题目】A、B、C、D、E、F是初中化学常见的六种物质,已知A为红棕色固体,A与F属于氧化物,D常用于改良酸性土壤,C是单质,其相互反应情况如下图所示(短线“—”相连的物质间能反应,箭头“→”表示能生成),上述反应均属于基本反应类型。

(1)B的浓溶液暴露在空气中质量会减少(不计水蒸发),B的俗称为_____。
(2)F→D的反应_____(填“放出”或“吸收”)热量。
(3)写出下列反应的化学方程式:
A→C:_____;
D→E:_____。
【答案】盐酸 放出 3C+Fe2O3![]() 2Fe+3CO2↑或3H2+Fe2O3
2Fe+3CO2↑或3H2+Fe2O3![]() 2Fe+3H2O Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
2Fe+3H2O Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
【解析】
A、B、C、D、E、F是初中化学常见的六种物质,已知A为红棕色固体,A与F属于氧化物,所以A是氧化铁,D常用于改良酸性土壤,所以D是氢氧化钙,C是单质,F会转化成氢氧化钙,所以F是氧化钙,E是碳酸钙,氧化铁会转化成铁,所以C是铁,B是稀盐酸,经过验证,推导正确。
(1)由分析可知,B的浓溶液暴露在空气中质量会减少,B的名称是盐酸;
(2)F→D的反应是氧化钙和水反应生成氢氧化钙,放出热量;
(3)A→C的反应是氧化铁和木炭或氢气在高温的条件下生成铁和二氧化碳,化学方程式为:3C+Fe2O3![]() 2Fe+3CO2↑或3H2+Fe2O3
2Fe+3CO2↑或3H2+Fe2O3![]() 2Fe+3H2O;
2Fe+3H2O;
D→E的反应是二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O。

【题目】探究醋蛋液
食用醋蛋液可以补充人体所需营养,做法(如下图):

将洗净的鸡蛋放入盛有7°白醋的玻璃杯中,放置3天左右,用筷子将蛋清与蛋黄打散即可。
(查阅资料)
食醋的主要成分为醋酸(CH3COOH),醋酸在水中能解离出H+和CH3COO-。
(提出问题)I.产生的气体是什么?
小英按照制作说明进行操作,把鸡蛋放入白醋中,观察到蛋壳逐渐溶解,表面有大量气泡产生,她对产生的气体进行了如下猜想:
(猜想与假设)
猜想1:二氧化碳 猜想2:氢气猜想 3:甲烷
(1)小英运用的观察方法是___________(填“直接”或“间接”)观察,小英在观察的基础上作出以上猜想的理论依据是____________。
(2)假设是利用已有的知识和经验进行加工处理形成的一种能被检验的假设性结论,其表述方式为:如果……,那么……针对以上任一种猜想做出你的假设:___________。
(获得结论)实验证明,产生的气体为二氧化碳。写出二氧化碳与澄清石灰水反应的化学方程式:_____________。
(反思与交流)
(3)将鸡蛋放入白醋中,蛋壳中的碳酸钙和醋酸作用生成可溶性的醋酸钙,可以补充人体所需钙元素。
II.醋蛋液中是否含有醋酸?
(实验探究)小英同学通过测定醋蛋液的酸碱度来确定其中是否含有醋酸,请将下表填写完整。
实验操作 | 实验现象及结论 |
________。 | 现象:_________。 结论:醋蛋液中含有醋酸。 |
(反思与交流)
(4)制得的醋蛋液中如果有过量的醋酸会为伤、腐蚀食道黏膜及损伤脾胃,食用时可加一定量的水进行稀释,加水稀释过程中醋蛋液的pH____________(填“增大”,“减小”或“不变”)。