题目内容
为设计验证锌、铁、铜三种金属的活动性顺序,每种方案所需试剂如下(反应所得产物可作下一步反应),其中不可行的方案是
- A.Fe、CuSO4溶液、ZnSO4溶液
- B.Zn、CuSO4溶液、FeSO4溶液
- C.Zn、Cu、FeSO4溶液
- D.Fe、Cu、ZnSO4溶液
D
分析:根据金属活动顺序进行思考,锌、铁、铜这三种金属的金属活动性由强到弱的顺序为锌>铁>铜.在金属活动顺序表中,前边的金属可以把后边的金属从其盐溶液中置换出来,所以可以选择相应的金属和盐溶液进行反应来证明这三种金属的活动性强弱.
解答:A、Fe、CuSO4溶液、ZnSO4溶液三种物质中,铁可以置换CuSO4溶液中的铜而出现红色固体,证明铁的活动性比铜强,铁和ZnSO4溶液不反应,证明锌比铁的活动性强,因此,可以证明三种金属的活动性强弱,故错误.
B、Zn、CuSO4溶液、FeSO4溶液三种物质中,锌可以置换CuSO4溶液中的铜而出现红色固体,证明锌的活动性比铜强,锌和FeSO4溶液也能反应,证明锌比铁的活动性强,把锌置换出的铁加入硫酸铜溶液中,有红色固体生成,说明铁的活动性比铜强,因此能证明三种金属的活动性强弱,故此项错误.
C、Zn、Cu、FeSO4溶液三种物质中,锌能与硫酸亚铁反应,证明锌比铁的活动性强,铜和硫酸亚铁不反应,证明铜的活动性比铁弱,也能得出三种金属的活动性强弱,故错误.
D、Fe、Cu、ZnSO4溶液三种物质中,铁和铜与硫酸锌溶液都不反应,证明锌的活动性比铁和铜强,但铁和铜的活动性强弱不能证明,因此此项也正确.
因此答案为:D
点评:同学们要会利用金属活动顺序表设计实验,去验证金属的活动性强弱.氢前边的金属会与酸反应,但氢后边的金属不会与酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.但也要注意,与金属反应酸一般是指稀硫酸和盐酸,不包括浓硫酸和硝酸.
分析:根据金属活动顺序进行思考,锌、铁、铜这三种金属的金属活动性由强到弱的顺序为锌>铁>铜.在金属活动顺序表中,前边的金属可以把后边的金属从其盐溶液中置换出来,所以可以选择相应的金属和盐溶液进行反应来证明这三种金属的活动性强弱.
解答:A、Fe、CuSO4溶液、ZnSO4溶液三种物质中,铁可以置换CuSO4溶液中的铜而出现红色固体,证明铁的活动性比铜强,铁和ZnSO4溶液不反应,证明锌比铁的活动性强,因此,可以证明三种金属的活动性强弱,故错误.
B、Zn、CuSO4溶液、FeSO4溶液三种物质中,锌可以置换CuSO4溶液中的铜而出现红色固体,证明锌的活动性比铜强,锌和FeSO4溶液也能反应,证明锌比铁的活动性强,把锌置换出的铁加入硫酸铜溶液中,有红色固体生成,说明铁的活动性比铜强,因此能证明三种金属的活动性强弱,故此项错误.
C、Zn、Cu、FeSO4溶液三种物质中,锌能与硫酸亚铁反应,证明锌比铁的活动性强,铜和硫酸亚铁不反应,证明铜的活动性比铁弱,也能得出三种金属的活动性强弱,故错误.
D、Fe、Cu、ZnSO4溶液三种物质中,铁和铜与硫酸锌溶液都不反应,证明锌的活动性比铁和铜强,但铁和铜的活动性强弱不能证明,因此此项也正确.
因此答案为:D
点评:同学们要会利用金属活动顺序表设计实验,去验证金属的活动性强弱.氢前边的金属会与酸反应,但氢后边的金属不会与酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.但也要注意,与金属反应酸一般是指稀硫酸和盐酸,不包括浓硫酸和硝酸.

练习册系列答案
相关题目
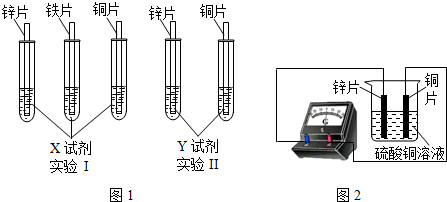
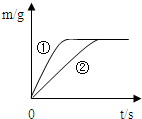 金属材料在生产、生活中的应用非常广泛.
金属材料在生产、生活中的应用非常广泛.